| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点整理《水的电离平衡》试题强化练习(2019年最新版)(二)
参考答案:(1)Al3+ +3H2O 本题解析:(1)NH4Al(SO4)2可作净水剂是因为溶于水时产生的Al3+发生水解生成有吸附性的Al(OH)3,能吸附水中的悬浮物,离子方程式为:Al3+ + 3H2O 本题难度:困难 2、填空题 常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如表所示:
(1)从甲组情况分析,如何判断HA是强酸还是弱酸? (2)乙组混合溶液中离子浓度c(A-)和c(Na+)的大小关系是 。 A.前者大 B.后者大 C.两者相等 D.无法判断 (3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是 。 (4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式): c(Na+)-c(A-)= mol・L-1。 参考答案:(1)a=7时,HA是强酸;a>7时,HA是弱酸 本题解析:(1)一元酸HA与NaOH等物质的量反应,酸性强弱取决于完全中和后盐溶液的pH,a=7时为强酸,a>7时为弱酸;(2)据电荷守恒,有c(Na+)+c(H+)=c(A-)+c(OH-),因c(H+)=c(OH-),所以c(Na+)=c(A-);(3)丙为等浓度的HA与NaA的混合溶液,由pH>7知A-水解程度大于HA的电离,离子浓度大小关系为c(Na+)>c(A-)>c(OH-)>c(H+);(4)据电荷守恒c(Na+)+c(H+)=c(A-)+c(OH-),推导c(Na+)-c(A-)=c(OH-)-c(H+)=10-4 mol/L-10-10 mol/L。 本题难度:困难 3、选择题 (10分)25℃时,有下列五种溶液: |
参考答案:(1) > , CO32- + H2O 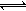 HCO3- + OH- (2) 1:1
HCO3- + OH- (2) 1:1
(3) 2Al3+ + 3CO32- + 3H2O ="=" 2Al(OH)3↓+ 3CO2↑ (4)C
本题解析:(1)0.1mol/L Na2CO3溶液,碳酸钠为强碱弱酸盐,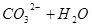
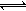
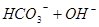 ,所以溶液呈碱性,PH>7;(2)氢氧化钠为强碱,硫酸为强酸,混合后PH=7,即恰好完全反应,
,所以溶液呈碱性,PH>7;(2)氢氧化钠为强碱,硫酸为强酸,混合后PH=7,即恰好完全反应,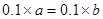 ,a:b =1:1;(3)Na2CO3溶液和Al2(SO4)3溶液发生双水解,反应的方程式为
,a:b =1:1;(3)Na2CO3溶液和Al2(SO4)3溶液发生双水解,反应的方程式为
2Al3+ + 3CO32- + 3H2O ="=" 2Al(OH)3↓+ 3CO2↑ ;(4)根据氯化银的溶度积,氯离子浓度越大,银离子浓度越小,故Ag+浓度最小的是0.1mol?L?1AlCl3溶液。
考点:本题考查弱电解质电离和盐的水解。
本题难度:一般
4、选择题 将pH=6的盐酸与pH=4的盐酸等体积混合,混合液中c(OH-)接近于
A.2×10-10 mol/L
B.(10-8+10-10)/2 mol/L
C.(10-8+10-4)/2 mol/L
D.(10-14+10-5) mol/L
参考答案:A
本题解析:
本题难度:一般
5、选择题 在10mL0.1mol・L-1NaOH溶液中加入同体积、同浓度的CH3COOH溶液,反应后溶液中各微粒的浓度关系错误的是
A.c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
B.c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
C.c(Na+)=c(CH3COO-)+c(CH3COOH)
D.c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
参考答案:A
本题解析:
答案:A
A、不正确,CH3COONa水解后呈碱性,c(Na+)>c(CH3COO-)>c(OH-)>c(H+);B、正确;C、正确,物料守恒;D、正确,电荷守恒。
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点归纳《与量有关的.. | |