1��ѡ���� ֻ��һ���Լ�������Na2SO4��MgCl2��FeCl2��Al2(SO4)3��FeCl3��CuSO4������Һ,�������Լ���
A.Ba(OH)2
B.H2SO4
C.NaOH
D.AgNO3
�ο��𰸣�C
��������������������������Һ�������Ӹ�����ͬ���ɴ������Ӽ���ĽǶȷ��������������ӣ��ɼ�����ϳ�������ɫ���������������ԵȽǶ��жϡ�����Ba(OH)2�������������ʶ���Ӧ���ҳ�������ɫ�е�����ͬ�ģ����ܼ��𣬹�A���������ᣬ�����������ʶ�����Ӧ�����ܼ��𣬹�B������NaOH��Na2SO4�������Ȼ�þ���ɰ�ɫ������FeCl2���ɰ�ɫ������Ѹ�ٱ�ɻ���ɫ������ܱ�ɺ��ɫ��Al2��SO4��3���ɰ�ɫ������NaOH����ʱ���������ܽ⡣�Ȼ������ɺ��ɫ������CuSO4������ɫ���������������ͬ���ɼ��𣬹�C��ȷ������AgNO3���������ʶ����ɰ�ɫ���������ܼ��𣬹�D����ѡC��
���㣺�������ʵļ���ͼ���Ļ�������
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⣬�����ۺ���ǿ�����ض�ѧ������������������ע������������ʵ�����ϵ���ͬ���ӷ�Ӧ���в�ͬ����ĽǶȿ��ǡ�����������Ҫ��ȷ�����ڽ������ʵļ���ʱ��Ҫ�������ʵ��������ʺ�������Ӧ��ѡ���ʵ����Լ��ͷ�����ȷ�۲췴Ӧ�е�������������ɫ�ı仯�����������ɺ��ܽ⡢����IJ�������ζ���������ɫ�ȣ������жϡ���������֤���ɡ�
�����Ѷȣ���
2������� �٢ڢۢܢ�����Ԫ�أ���Ԫ�����ڱ��е�λ����ͼ��ʾ���ش��������⣺?
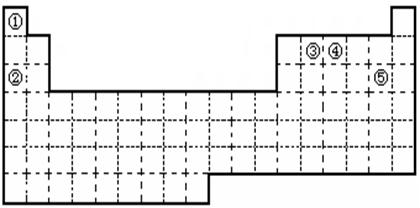
��1���٢ڢۢܢ�����Ԫ���У���������ǿ��Ԫ����?��дԪ�����ƣ��� ��Ԫ�صĵ����ڿ�����ȼ�յĻ�ѧ����ʽΪ?����?��
��2��Ԫ�آڵ�����������Ӧ��ˮ��������?�����������ۡ������ӡ� ���������ʽΪ ?�� �ԱȽϢں͢�ԭ�Ӱ뾶�Ĵ�С
��?�ۣ������ ���� ��
��3������Ԫ�آܵ�ԭ�ӽṹʾ��ͼ?����Ԫ�ص�����������
ˮ��������Cu������Ӧ����Ӧ�������������ǣ�д��ѧʽ��?��
��4��д��Ԫ�آ������ڱ��е�λ��?���Ժ�ˮ�к�����������Ϊԭ�Ͽ��������ݵĵ��ʣ�ͬʱ�����Եõ�����������Ҫ�Ĺ�ҵԭ�ϣ��÷�Ӧ�Ļ�ѧ����ʽΪ?����?��
��5�����мס������ֶ�����Ԫ�أ������£���Ԫ�ص��������Ũ���������У����涼�������ܵ�����Ĥ����Ԫ��ԭ�Ӻ���L���������M���������4����
�ټס���Ԫ�طֱ�Ϊ??�� ?��дԪ�����ƣ�
��д���ڵ�����������Ӧ��ˮ���������������ﷴӦ�����ӷ���ʽ??
�ο��𰸣���1�� �� ��1�֣�?2Na + O2  ?Na2O2��2�֣�
?Na2O2��2�֣�
��2�� ����?����ʽ��?��?����1�֣�?
���
?��3��?�ԣ�? HNO3����1�֣�?��4�� �������ڢ�A �� ��1�֣�2NaCl ��2H2O ��Cl2����H2����2NaOH��2�֣�
��5��������þ����1�֣�?
��2NaOH��Al2O3��2Na AlO2��H2O��2�֣�
�������������Ԫ���������ڱ��е�λ�ÿ�֪����ΪHԪ�أ���ΪNaԪ�أ���ΪCԪ�أ���ΪNԪ�أ���ΪClԪ�ء�
��1��ͬ������Ԫ�صĽ����Դ�����������ͬ����Ԫ�صĽ����Դ��ϵ�������ǿ�����������ǿΪNa����������ȼ�յĻ�ѧ����ʽΪ2Na + O2  ?Na2O2��
?Na2O2��
��2��Ԫ�آڵ�����������Ӧ��ˮ����ΪNaOH��Ϊ���ӻ��������ʽΪ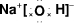 ���Ƶ�ԭ�Ӻ�����3�����Ӳ㣬C��ԭ�Ӻ�����2�����Ӳ㣬������Ӳ���Խ�࣬�뾶Խ�ʢڣ��ۣ�
���Ƶ�ԭ�Ӻ�����3�����Ӳ㣬C��ԭ�Ӻ�����2�����Ӳ㣬������Ӳ���Խ�࣬�뾶Խ�ʢڣ��ۣ�
��3����ΪNԪ�أ�ԭ�Ӻ�����2�����Ӳ㣬����������Ϊ5��ԭ�ӽṹʾ��ͼΪ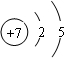 �����Ӧ������������ˮ����ΪHNO3������ǿ�����ԣ���ͭ��Ӧʱ����������
�����Ӧ������������ˮ����ΪHNO3������ǿ�����ԣ���ͭ��Ӧʱ����������
���
?��4����ΪClԪ�أ�ԭ�Ӻ�����3�����Ӳ㣬����������Ϊ7�������ڵ������ڢ�A�壬��ⱥ��ʳ��ˮ�IJ���Ϊ�������ơ���������������Ӧ�ķ���ʽΪ2NaCl+2H2O��Cl2����H2����2NaOH����5���ټ�Ԫ�ص��������Ũ���������У����涼�������ܵ�����Ĥ�������ۻ���Ӧ��ӦΪ�����ʣ���Ԫ��ԭ�Ӻ���L���������M���������4����ӦΪþԪ�أ��ʴ�Ϊ������þ���ڵ�����������Ӧ��ˮ����������������ķ�ӦΪ�������ƺ��������ķ�Ӧ��������Ϊ������������������Ʒ�Ӧ����ƫ�����ƺ�ˮ����Ӧ�Ļ�ѧ����ʽΪ
2NaOH+Al2O3��2NaAlO2+H2O��
���������⿼���Ϊ�ۺϣ��漰Ԫ�ص��ƶϡ�Ԫ�������ɡ�������ԭ��Ӧ������Լ���ѧ��Ӧ�����������⣬��Ŀ�Ѷ��еȣ�ע����ȷ����Ԫ�������ɵĵݱ�����Լ���ػ���֪֮ʶ�Ļ��ۣ�
�����Ѷȣ�һ��
3��ѡ���� һ����ij���ʵ���Һ������������Ϊ0.2A��������������ˮϡ�ͺ�����������С��0.1A�������Һ���ܶ�
A.����ˮ���ܶ�
B.С��ˮ���ܶ�
C.����ˮ���ܶ�
D.��ȷ��
�ο��𰸣�B
���������
�����Ѷȣ�����
4��ѡ���� �ס���Ϊ������Ԫ�صĵ��ʣ�������Ϊ��������Ǵ�������ת����ϵ��
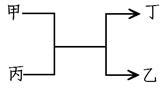
����ҿ�����
A���ƺ�����
B��þ��̼
C����������
D��������
�ο��𰸣�B
���������ѡ��A������ΪNa����ΪH2�����ΪH2O����ΪNaOH��NaOH����������������⡣ѡ��B������ΪMg����ΪC�����ΪCO2����ΪMgO���������⡣ѡ��C������ΪO2����ΪS�����ΪH2S����ΪH2O��H2S������������������⡣ѡ��D�������Ƕ�����Ԫ�أ����������⡣
�����Ѷȣ�һ��
5��ѡ���� X��Y��Z��W��Ϊ������Ԫ�أ����������ڱ��е�λ������ͼ��ʾ����Xԭ�ӵ��������������������������3��������˵���������(? )
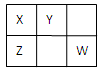
A��ԭ�Ӱ뾶��Z>X>Y
B������������Ӧˮ��������ԣ�Z>W
C������Ԫ�ص��⻯���У�Y���⻯��е����
D�������ӵĻ�ԭ�ԣ�Z<W
�ο��𰸣�BD
�������������Ԫ�������ڱ��е�λ�ÿ��жϣ�X�ǵڶ����ڡ�Xԭ�ӵ��������������������������3��������X�ǵ�Ԫ�ء���Y����Ԫ�أ�Z����Ԫ�أ�W����Ԫ�ء�ͬ�������϶���ԭ�Ӱ뾶��������������ǿ���ǽ���������������������ˮ���������������ͬ�����������ң�ԭ�Ӱ뾶��С���������������ǽ���������ǿ������A��ȷ��B����ȷ������������Ӧˮ���������Ӧ����W>Z��ˮ�к�����������Էе���ߣ�C��ȷ���ǽ�����Խǿ����Ӧ�����ӵĻ�ԭ�Ծ�Խ��������D����ȷ�������ӵĻ�ԭ����Z��W����ѡBD��
�����Ѷȣ�һ��