1、实验题 如图所示A~H为实验室常见的仪器、装置(部分固定夹持装置略去),请根据要求回答下列问题
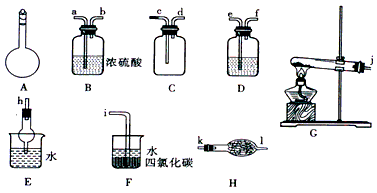
(1)A仪器的名称是_____________,常用于_____________。
(2)用图中所示仪器设计一套制取一瓶干燥、纯净氨气的实验装置,仪器的连接顺序是(用管口字母符号表示):j接__________________________。
为了研究Cl2的性质,设计如图所示装置进行实验(装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸)。
(3)加入药品前,检查Ⅰ中气体发生装置气密性的操作是_________________________________
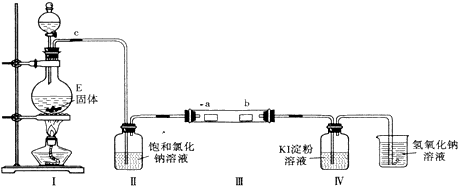
(4)实验过程中,装置Ⅳ中的实验现象为________________________。
(5)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化“这一预期现象。为了达到这一实验目的,你认为应在__________之间(选填装置序号)还需添加一个洗气瓶,该装置的作用是__________________________。
参考答案:(1)容量瓶;配制一定物质的量浓度的溶液
(2)j接k,l接d,c接h或I
(3)用止水夹夹住C处橡皮管,然后向分液漏斗中加水,打开分液漏斗活塞,有液体液面高于烧瓶液面,但不流下,则气密性好
(4)无色液体变蓝色
(5)Ⅱ、Ⅲ;干燥氯气
本题解析:
本题难度:困难
2、选择题 将0.03mol Cl2缓缓通入含有0.02mol H2SO3和0.02mol HBr的混合溶液中,在此过程中C(H+)与Cl2用量的关系是
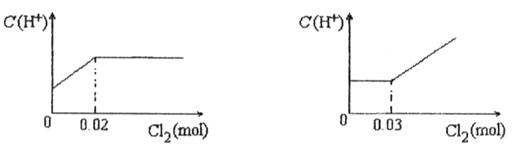
A? B
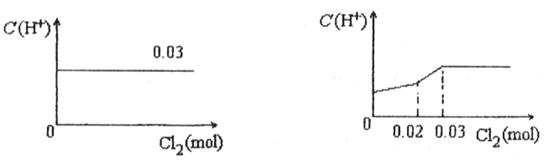
C? D
参考答案:A
本题解析:略
本题难度:一般
3、选择题 氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是(?)
A.再通入少量氯气,c(H+)/c(ClO-)减小
B.通入少量SO2,溶液漂白性增强
C.加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-)
D.加入少量固体NaOH,溶液的pH会略微增大
参考答案:D
本题解析:Cl2与水发生反应:Cl2+H2O H++Cl-+HClO,反应达平衡后,再通入Cl2,溶液仍然是饱和溶液,各离子浓度以及离子浓度比均不发生变化;通入SO2发生反应:Cl2+SO2+2H2O=2HCl+H2SO4,故溶液漂白性降低;往氯水中加入少量NaOH固体,溶液pH会增大,且溶液中存在电荷守恒:
H++Cl-+HClO,反应达平衡后,再通入Cl2,溶液仍然是饱和溶液,各离子浓度以及离子浓度比均不发生变化;通入SO2发生反应:Cl2+SO2+2H2O=2HCl+H2SO4,故溶液漂白性降低;往氯水中加入少量NaOH固体,溶液pH会增大,且溶液中存在电荷守恒:
c(Na+)+c(H+)=c(OH-)+c(Cl-)+c(ClO-),由于NaOH固体少量,故溶液显酸性,c(H+)>c(OH-),所以c(Na+)<c(Cl-)+c(ClO-)。
本题难度:一般
4、计算题 现有某纯净气体A,取标准状况下体积均为2.24L的两份样品,一份与过量的O2混合,燃烧后无固体物质生成,气体生成物均被过量的澄清石灰水吸收,得到13.90g沉淀。另一份在标准状况下与一定质量的SO2气体混合(A不与SO2反应),测得混合气体对H2的相对密度为20。试推测A是什么?并写出A完全燃烧反应方程式。
参考答案:A为CH3F?完全燃烧时的反应方程式为2CH3F+3O2 2CO2+2H2O+2HF
2CO2+2H2O+2HF
本题解析:① =20×2=40,故MA<40;
=20×2=40,故MA<40;
②A气体为0.1mol,若生成的气体为CO2,则生成CaCO3的沉淀质量应为10g,20g……显然与题意不符;
③若生成气体为SO2,生成CaSO3,其质量应为12g,24g……显然也与题目不相符;
④若既生成CaCO3沉淀又生成CaSO3沉淀,是否可行呢?也不行,因为A中若含C、S两元素,其相对分子质量已大于40;
⑤只能从Ca2+相应的难溶性盐进行思维发散:有CaF2、CaSiO3、Ca3(PO4)2等;
⑥思维辐合:CaSiO3、Ca3(PO4)2与题意不符,因为在燃烧时硅、磷变成了固体氧化物;
⑦只含F是不行的;
⑧很可能既含有C、又含有F的F卤代烃,且都只有一个原子(因受相对分子质量的制约);
⑨代入求算,生成的沉淀恰好为13.90g;
⑩最后确定A的分子式为CH3F。
本题难度:一般
5、简答题 如图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加2滴浓盐酸后,立即用另一培养皿扣在上面.
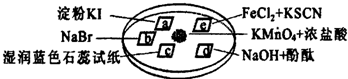
已知:2KMnO4+16HCl→2KCl+5Cl2↑+2MnCl2+8H2O对实验现象的“解释或结论”正确的是:
(1)a处变______色,b处变______色;
(2)c处的现象为______,请说明原因______;
(3)e处变______色,反应的离子方程式为______、______;
(4)近年来科学家提出,高铁酸钾(K2FeO4)也可用作水处理剂.可用FeCl3与KClO在强碱性条件下反应制取,其反应的离子方程式为(不需要配平)______.
参考答案:(1)Cl2分别与KI、NaBr作用生成I2、Br2,a处变蓝、b处变橙色,故答案为:蓝;橙;
(2)氯气与水反应Cl2+H2O=H++Cl-+HClO,H+使试纸变红,HClO具有漂白性,可使试纸褪色,则C处先变红,后褪色,故答案为:先变红后褪色;Cl2+H2O=H++Cl-+HClO;H+使试纸变红,HClO使试纸褪色;
(3)Cl2将Fe2+氧化为Fe3+,试纸变为红色,反应的离子方程式2Fe2++Cl2=2Fe3++2Cl-;Fe3++3SCN-=Fe(SCN)3,
故答案为:红;2Fe2++Cl2=2Fe3++2Cl-;Fe3++3SCN-=Fe(SCN)3;
(4)用FeCl3与KClO在强碱性条件下反应制取K2FeO4,反应的离子方程式为2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O,
故答案为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O.
本题解析:
本题难度:一般