1、选择题 我国的“神舟五号”载人飞船已发射成功,“嫦娥”探月工程也已正式启动。据科学家预测,月球的土壤中吸附着数百万吨的 ,每百吨
,每百吨 核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氦元素主要以
核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氦元素主要以 的形式存在。下列说法正确的是
的形式存在。下列说法正确的是
[? ]
A. 原子核内含有4个质子
原子核内含有4个质子
B. 和
和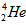 互为同位素
互为同位素
C.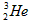 原子核内含有3个中子
原子核内含有3个中子
D.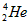 的最外层电子数为2,有较强的金属性
的最外层电子数为2,有较强的金属性
2、选择题 下列化学用语正确的是
[? ]
A.硫的原子结构示意图: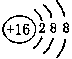
B.顺-2-丁烯的结构简式: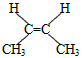
C.乙酸的实验式:C2H4O2
D.原子核内有8个中子的氧原子:188O
3、推断题 四种常见元素:A、B、C、D为周期表前四周期元素,原子序数依次递增,它们的性质或结构信息如下表。试根据信息回答有关问题。
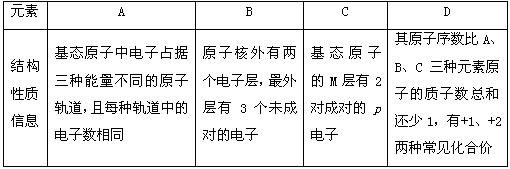
(1)写出D原子的外围电子排布式________,A、B、C、D四种元素的第一电离能最小的是_______(用元素符号表示)。
(2)B元素的氢化物的沸点比同主族相邻元素氢化物沸点______(填“高”或“低”)。
(3) 元素F与A相邻且同主族,它们与氧元素的成键情况如下
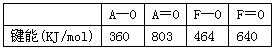
在A和O之间通过双键形成AO2分子,而F和O则不能和A那样形成有限分子,原因是___________________________。
(4)往D元素的硫酸盐溶液中逐滴加入过量B元素的氢化物水溶液,可生成的配合物,该配合物中不含有的化学键是____________(填序号)。
a.离子键 b.极性键 c.非极性键 d.配位键 e.金属键
(5)下列分子结构图中的“ ”表示上述相关元素的原子中除去最外层电子的剩余部分,“
”表示上述相关元素的原子中除去最外层电子的剩余部分,“ ”表示氢原子,小黑点“
”表示氢原子,小黑点“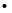 ”表示没有形成共价键的最外层电子,短线表示共价键。
”表示没有形成共价键的最外层电子,短线表示共价键。
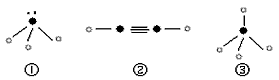
则在以上分子中,中心原子采用sp3杂化形成化学键的是________(填序号);在②的分子中有______个σ键和_______个π键。
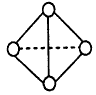
(6)已知一种分子B4分子结构如图所示,断裂1molB-B吸收aKJ的热量,生成1molB≡B放出bKJ热量。试计算反应:B4(g)==2B2(g) △H=_______kJ/mol。
4、选择题 关于ⅤA族元素(用R代表)的叙述正确的是( )
A.最高化合价是+5
B.氢化物的通式为RH5
C.非金属性由上到下递增
D.其含氧酸均为一元强酸
5、填空题 原子序数依次增大的四种短周期元素A、B、C、D,其中A与D同主族,B与C同周期,A、D原子的最外层电子数都是1,B原子最外层电子数是次外层电子数的2倍,C原子最外层电子数比B原子多2个。A、C单质在常温下均为气体,它们在点燃下以体积比2∶1完全反应,生成物在常温下是液体。此液体与D单质能激烈反应生成A的单质,所得溶液滴入酚酞显红色,同时溶液中含有与氖原子的电子层结构相同的两种离子。回答下列问题:
⑴、写出BC2的电子式?______ ,结构式?______ 。
⑵、A、C、D元素形成的化合物中含有的化学键的类型为____? ,该物质的晶体类型是?__ 。
⑶、写出一种由A、B、C、D四种元素共同组成的化合物的化学式?____ 。