1、填空题 (15分) 下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
a
| ?
| ?
|
b
| ?
| ?
| ?
| c
| d
| e
| f
| ?
|
g
| h
| i
| j
| ?
| k
| l
| m
|
n
| ?
| ?
| ?
| ?
| ?
| ?
| o
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
| | | | | | | | | | | | | | | | |
|
试回答下列问题:
(1)请写出元素O的基态原子电子排布式??。
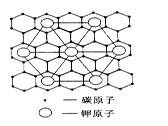
(2)c元素的一种同素异形体与熔融的n单质形成石墨间隙化合物,比较常见的石墨间隙化合物是青铜色的化合物,其化学式可写作CxK,其平面图形见图,则x值为?。
(3)第三周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表?(填元素符号);其中电负性最大的是?(填图中的序号)。

(4)由i原子跟d原子以1 : 1相互交替结合而形成的晶体,晶型与晶体j相同。则i与d形成的晶体中一个晶胞中含有4个i原子;与同一个i原子相连的d原子构成的空间构型为?,d原子的杂化类型为?。
(5)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
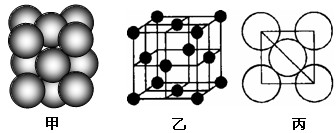
若已知i的原子半径为dcm,NA代表阿伏加德罗常数,i的相对原子质量为M,
则该晶体的密度为______?_g/cm3?(用字母表示)。
2、选择题 随着科学 技术的不断进步,研究物质的手段和途径越来越多,N
技术的不断进步,研究物质的手段和途径越来越多,N 、H3、O4、C60等已被发现。下列有关说法中,正确的是?(?)
、H3、O4、C60等已被发现。下列有关说法中,正确的是?(?)
A.N 中含有36个电子
中含有36个电子
B.O2和O4属于同位素
C.C60晶体是原子晶体
D.H2和H3属于同素异形体
3、实验题 某学生在做元素性质与原子结构关系的实验时,设计了一套实验方案,并记录了有关的实验现象。请帮助该学生整理并完成实验报告。
(1)实验目的
探究同一主族元素性质的递变规律。
(2)实验用品
仪器:试管、胶头滴管
药品:新制氯水、新制溴水、溴化钠溶液、碘化钠溶液、四氯化碳
(3)实验内容(在下表横线中填写相关内容)
序号
| 实验方案
| 实验现象
|
①
| 向盛有少量溴化钠溶液的试管中滴加少量新制氯水,振荡,再加入少量四氯化碳,振荡后静置
| 液体分为两层,下层呈_____色
|
②
| 向盛有少量碘化钠溶液的试管中滴加少量新制溴水,振荡,再加入少量四氯化碳,振荡后静置
| 液体分为两层,下层呈_____色
|
?
(4)实验结论:_________________________________。
(5)问题和讨论
①上述两个实验中发生反应的离子方程式分别为________________、__________________。
②由于氟单质过于活泼,所以很难设计出一个简单的实验来验证其氧化性的强弱。试列举两项事实说明氟的非金属性比氯的强:______________、______________。
4、选择题 据报载我国最近合成新的同位素,其中一种是72 Hf(铪),它的质量数是(?)
A.72
B.113
C.185
D.257
5、选择题 化学概念和物质的分类在逻辑上存在包含、并列、交叉等关系,下列选项中前者包含后者的是
A.酸、碱
B.化合物、电解质
C.溶液、胶体
D.氧化还原反应、分解反应