1、填空题 工业上制备BaCl2的工艺流程图如下
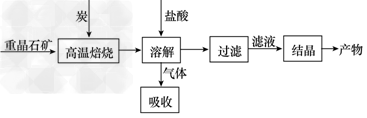
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得
BaSO4(s)+4C(s) 4CO(g)+BaS(s) ΔH1=571.2?kJ/mol ①
4CO(g)+BaS(s) ΔH1=571.2?kJ/mol ①
BaSO4(s)+2C(s) 2CO2(g)+BaS(s) ΔH2=226.2?kJ/mol ②
2CO2(g)+BaS(s) ΔH2=226.2?kJ/mol ②
(1)气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为__________________________________________。
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时, =________。
=________。
[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
(3)反应C(s)+CO2(g) 2CO(g)的ΔH3=____kJ/mol。
2CO(g)的ΔH3=____kJ/mol。
(4)实际生产中必须加入过量的炭,同时还要通入空气,其目的是__________________________________________________。
参考答案:(1)S2-+H2O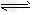 HS-+OH-、HS-+H2O
HS-+OH-、HS-+H2O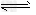 H2S+OH-
H2S+OH-
(2)2.7×10-3
(3)172.5
(4)使BaSO4得到充分还原(或提高BaS的产量);①②为吸热反应,炭和氧气反应放热可维持反应所需高温
本题解析:
本题难度:一般
2、选择题 将足量的BaCO3粉末分别加入下列溶液中,充分溶解至溶液饱和.各溶液中Ba2+的浓度最小的为( )
A.10?mL?0.2?mol/LNa2CO3溶液
B.40?mL水
C.50?mL?0.01?mol/L?氯化钡溶液
D.100?mL?0.01?mol/L盐酸
参考答案:A.将足量BaCO3粉末加入10mL0.2mol/LNa2CO3溶液中,由于碳酸根离子的浓度较大,抑制碳酸钡的溶解,则Ba2+的浓度很小;
B.BaCO3粉末加入40mL水中,充分溶解至溶液饱和存在BaCO3(s)?Ba2+(aq )+CO32-(aq),则溶液中存在一定浓度的Ba2+,但浓度较小;
C.将足量BaCO3粉末加入50mL0.01mol/L氯化钡溶液中,氯化钡电离产生0.01mol/LBa2+,则Ba2+的浓度较大;
D.将足量BaCO3粉末加入100mL0.01mol/L盐酸中,碳酸钡与盐酸反应生成0.005mol/LBa2+,则Ba2+的浓度较大;
显然A中Ba2+的浓度最小,
故选A.
本题解析:
本题难度:一般
3、选择题 把Ca(OH)2固体放入一定量的蒸馏水中,一定温度下达到平衡:Ca(OH)2(s)?Ca2+(aq)+2OH-(aq).当向悬浊液中加入少量生石灰后,若温度保持不变,下列判断正确的是( )
A.溶液的pH增大
B.溶液的pH不变
C.溶液中Ca2+数目增多
D.溶液中c(Ca2+)增大
参考答案:向悬浊液中加少量生石灰,发生:CaO+H2O=Ca(OH)2,
AB.反应后仍为饱和溶液,c(OH-)不变,溶液pH不变,故A错误,B正确;
C.加入CaO,消耗水,由于原溶液已达到饱和,则平衡向逆反应方向移动,溶液中Ca2+数目减少,故C错误;
D.反应后仍为饱和溶液,c(Ca2+)不变,故D错误;
故选B.
本题解析:
本题难度:简单
4、选择题 下列各项中的两个量,其比例为2:1的是(?)
A.pH=7的氨水与(NH4)2SO4的混合溶液中,c(NH4+)与c(SO42-)之比
B.同温度下,0.2mol/LCH3COOH溶液与0.1mol/L CH3COOH溶液中的c(H+)之比
C.液面在“0”刻度,50mL酸式滴定管和25mL酸式滴定管内所盛溶液的体积
D.0.2mol/L的NaHSO3溶液中的阳离子与阴离子的浓度之比
参考答案:A
本题解析:略
本题难度:简单
5、选择题 难溶电解质AB2饱和溶液中,c(A2+)=x mol?L-1,c(B-)=y mol?L-1,则Ksp(AB2)值为( )
A.
xy2
B.xy
C.xy2
D.4xy2
参考答案:难溶电解质AB2的电离方程式为:AB2(S)?A 2+(aq)+2 B-(aq),
AB2饱和溶液中,c(A2+)=xmol?L-1,c(B-)=ymol?L-1,
则Ksp=c(A 2+).c2( B-)=xy2,
故选C.
本题解析:
本题难度:简单