|
|
|
高考化学必考知识点《难溶电解质的溶解平衡》高频考点预测(2019年最新版)(五)
2020-07-08 01:58:20
【 大 中 小】
|
1、选择题 25℃时,用Na2S沉淀Cu2+、Mn2+、Fe2+、Zn2+四种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)关系如图所示。下列说法正确的是
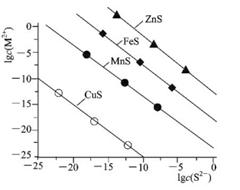
A.Ksp(CuS)约为l×10-20
B.向Cu2+浓度为10-5mol?L-1废水中加入ZnS粉末,会有CuS沉淀析出
C.向l00mL浓度均为10-5mol?L-1 Zn2+、Fe2+、Mn2+的混合溶液中逐滴加入10-4mol?L-1 Na2S溶液,Zn2+先沉淀
D.Na2S溶液中:2c(S2-)+2c(HS-)+2c(H2S)=c(Na+)
|
2、选择题 一定温度下,石灰浆中存在下列平衡:Ca(OH)2(s)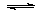 Ca2+(aq)+2OH-(aq),当向一定量的石灰浆中加入少量生石灰后并恢复到原来的温度,下列说法正确的是 Ca2+(aq)+2OH-(aq),当向一定量的石灰浆中加入少量生石灰后并恢复到原来的温度,下列说法正确的是
A.溶液中Ca2+离子数目减少
B.溶液中c(Ca2+)增大
C.溶液的pH增大
D.溶液中溶质的质量分数增大
|
3、填空题 (8分)(1)粗制的CuCl2・2H2O晶体中常含有Fe3+、Fe2+杂质。在提纯时,常先加入合适的氧化剂,将Fe2+氧化为Fe3+,下列可选用的氧化剂是___________。
A.KMnO4 B.H2O2 C.Cl2水 D.HNO3
(2)己知:常温下Ksp[Fe(OH)3]=8.0×10-38,Ksp[Cu(OH)2]=2.2×10-20,
4、选择题 已知25 。C时,AgI饱和溶液中c(Ag+)为1.22×10-8 mol/L,AgCl的饱和溶液中c(Ag+)为 1.25×10-5 mol/L。若在5 mL含有KCl和KI各为0.01 mol/L的溶液中,加入8 mL 0.01 mol/L AgNO3溶液,这时溶液中所含溶质的离子浓度大小关系正确的是
[? ]
A.c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-)
B.c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-)
C.c(NO3-)>c(K+)>c(Ag+)>c(Cl-)>c(I-)
D.c(K+)>c(NO3-)>c(Ag+)=c(Cl-)+c(I-)
5、填空题 阅读下表中短周期主族元素的相关信息。 请回答

(1)在一定条件下,B2与C的单质在海水中可形成原电池,为新型海水航标灯提供能源。写出该原电池正极的电极反应式_____________
(2)用惰性电极电解化合物AD的水溶液,该反应的化学方程式为:_________;其中,阴极产物是__________
(3)常温下,0.1 mol・L-1 X溶液的pH_________7(填“>”“=”或“<”),原因是 _____________(用离子方程式说明)。
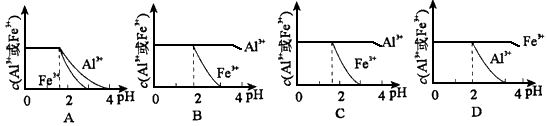
(4)已知Ksp[Al(OH)3]=1.3×10-33,Ksp[Fe(OH)3]=4.0×10 -38。现向pH=0,浓度均为0.04 mol・L-1的Al3+ 、Fe3+溶液中加入A的最高价氧化物对应水化物的溶液,以调节pH(设溶液体积不变),该过程中Al3+、Fe3+的浓度与pH关系正确的是______________(填字母代号)。