1、选择题 某二价金属的碳酸盐和碳酸氢盐的混合物跟足量盐酸反应时消耗的H+和产生CO2的物
质的量之比为5∶4,该混合物中碳酸盐和碳酸氢盐的物质的量之比为
A.1∶2
B.2∶3
C.3∶4
D.4∶5
参考答案:B
本题解析:设二价金属为M,混合物中碳酸盐(MCO3)和碳酸氢盐〔M(HCO3)2〕的物质的量分别为x和y,由题意可知:







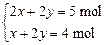 ?解得
?解得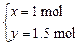 ?x∶y=2∶3
?x∶y=2∶3
本题难度:简单
2、实验题 晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:
①高温下用过量的碳还原二氧化硅制得粗硅,同时得到一种可燃性气体;
②粗硅与干燥的HCl气体反应制得SiHCl3(Si+3HCl SiHCl3+H2);
SiHCl3+H2);
③SiHCl3与过量的H2在1 100~1 200 ℃的温度下反应制得纯硅,已知SiHCl3能与水剧烈反应,在空气中易自燃。
请回答:
(1)第一步制取粗硅的化学反应方程式为?。
(2)粗硅与HCl气体反应完全后,经冷凝得到的SiHCl3(沸点33.0 ℃)中含有少量SiCl4(沸点57.6 ℃)和HCl(沸点-84.7 ℃),提纯SiHCl3采用的方法为?。
(3)实验室用SiHCl3与过量的H2反应制取纯硅装置如图所示(加热和夹持装置略去):
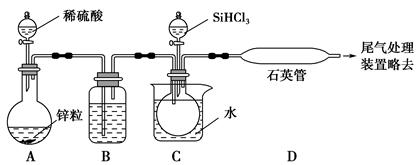
①装置B中的试剂是?,装置C中的烧杯需要加热,目的是?。
②反应一段时间后,装置D中观察到的现象是?,装置D不能采用普通玻璃管的原因是?,装置D中发生反应的化学方程式是?。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及?。
参考答案:(1)SiO2+2C Si+2CO↑
Si+2CO↑
(2)分馏(或蒸馏)
(3)①浓硫酸 使滴入烧瓶中的SiHCl3汽化
②有固体物质生成 在题给反应温度下(1 100~1 200 ℃),普通的玻璃会软化
SiHCl3+H2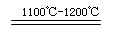 Si+3HCl
Si+3HCl
③排尽装置中的空气
本题解析:(3)①因SiHCl3与水强烈反应,故A中产生的H2必须干燥,因此B中的试剂为浓H2SO4,且C烧瓶需加热,其目的是使SiHCl3汽化,加快其与H2的反应速率。②石英管中产生的物质应为硅,故D中有固体产生,由题给信息,制纯硅的反应条件为1 100~1 200 ℃,此温度下普通的玻璃容易软化。③因高温下H2与O2反应容易爆炸,故还应排尽装置中的空气。
本题难度:一般
3、判断题 有三种透明、不溶于水的坚硬固体。A固体在氧气中完全燃烧只得到一种无色无味气体,此气体能使澄清石灰水变浑浊,标准状况下测得此气体的密度是氧气密度的1.375倍。B固体能溶于热的苛性钠溶液,再往该溶液中加入过量盐酸时,析出白色沉淀,此沉淀是一种比H2CO3还弱的酸,干燥后为不溶于水的白色粉末。B与石灰石、纯碱按一定比例混合加热后,能得到C,C在高温时软化,无固定熔点。根据以上事实,判断A、B、C各为何物,写出有关反应的化学方程式。
参考答案:A为金刚石、B为石英、C为普通玻璃。有关的化学方程式如下:
C+O2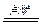 CO2,CO2+Ca(OH)2=CaCO3↓+H2O; SiO2+2NaOH=Na2SiO3+H2O;
CO2,CO2+Ca(OH)2=CaCO3↓+H2O; SiO2+2NaOH=Na2SiO3+H2O;
Na2SiO3+2HCl+H2O=H4SiO4↓+2NaCl; H4SiO4=H2SiO3+H2O;
CaCO3+SiO2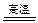 CaSiO3+CO2↑; SiO2+Na2CO3
CaSiO3+CO2↑; SiO2+Na2CO3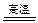 Na2SiO3+CO2↑
Na2SiO3+CO2↑
本题解析:A物质燃烧后产生气体的相对分子质量为:32×1.375=44。结合它无色无味且使澄清石灰水变浑浊的性质,可推断此气体为CO2,又因为A为透明不溶于水的坚硬固体,故可判断A为金刚石。方程式为: C+O2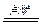 CO2。
CO2。
B物质能与苛性钠反应,且所得溶液与盐酸反应生成一种比H2CO3还弱的酸,且这种酸是一种难溶于水的白色固体,故可判断B为石英。相关方程式为: SiO2+2NaOH=Na2SiO3+H2O; Na2SiO3+2HCl+H2O=H4SiO4↓+2NaCl; H4SiO4=H2SiO3+H2O。
C物质由石灰石、纯碱、B物质(石英)混合加热而制得,结合高温时软化且无固定熔点,判断C物质为普通玻璃。相关方程式为:SiO2+CaCO3 CaSiO3+CO2↑;SiO2+Na2CO3
CaSiO3+CO2↑;SiO2+Na2CO3 Na2SiO3+CO2↑。
Na2SiO3+CO2↑。
本题考查有关SiO2、Na2SiO3、H2SiO3以及玻璃等物质的性质以及推理判断能力。其突破口是C高温时软化,无固定熔点,这是玻璃的特性,由此推知B可能为SiO2是解题的关键。
本题难度:简单
4、计算题 普通玻璃的主要成分为Na2SiO3・CaSiO3・4SiO2
(1)试计算普通玻璃中相当含有Na2O,CaO和SiO2的质量分数各是多少?
(2)制造50kg普通玻璃,需要纯碱、碳酸钙和二氧化硅各多少千克?
参考答案:(1)普通玻璃中Na2O的质量分数为13%,CaO的质量分数为11.7%,SiO2质量分数为75.3%。
(2)制造50kg普通玻璃,需要纯碱11.11kg、碳酸钙10.45kg、二氧化硅37.65kg。
本题解析:Na2SiO3・CaSiO3・4SiO2可用二氧化硅和金属氧化物的形式表示其组成为:Na2O・CaO・6SiO2。
(1)Na2O的摩尔质量为62g/mol,CaO的摩尔质量为56g/mol,SiO2的摩尔质量为60g/mol。
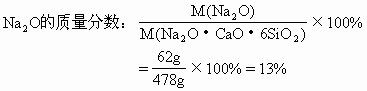
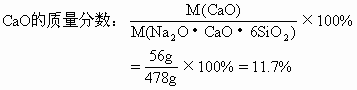
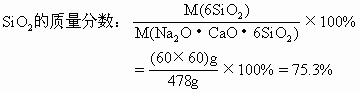
(2)由第(1)题求出普通玻璃中各氧化物的质量分数,可计算50kg普通玻璃中Na2O、CaO和SiO2的含量:
m(Na2O):50kg×13%=6.5kg
m(CaO):50kg×11.7%=5.85kg
m(SiO2):50kg×75.3%=37.65kg
再求需纯碱、碳酸钙和二氧化硅的质量:
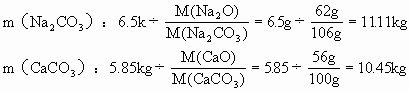
m(SiO2):37.65kg
本题难度:一般
5、选择题
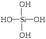
2H4SiO4====H6Si2O7+H2O所得H6Si2O7分子中Si―O键的数目是
A.4
B.6
C.7
D.8
参考答案:D
本题解析:两分子原硅酸失水形成H6Si2O7的过程可表示如下:
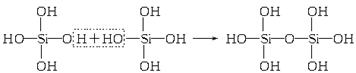
则所得H6Si2O7中所含硅氧键的数目为8个,即D项正确。
本题难度:简单