1、选择题 下列叙述正确的是(?)
A.能证明碳酸的酸性比硅酸强的事实是:CO2溶于水生成碳酸,SiO2不溶于水也不能跟水直接反应生成硅酸
B.太阳能电池可采用硅材料制作,其应用有利于环保、节能
C.人造刚玉熔点很高,可用作高级耐火材料,主要成分是二氧化硅
D.自然界中既存在化合态的硅又存在游离态的硅
2、填空题 “蛇纹石石棉”主要成分有二氧化硅、氧化镁和结晶水,它的化学式是Mg6[(OH)4Si2O5]2。
(1)“蛇纹石石棉”的氧化物形式为______________________,其中原子半径最大的元素
在周期表中的位置是______________________。
(2)Si原子的最外层的电子排布式为_____________,SiO2与NaOH溶液反应的化学方程式
为________________________________________________。
(3) SiCl4比SiO2的熔点_____(填“低”、“高”),原因是__________________________。
(4)从哪些方面不能判断Si和O的非金属性强弱?。
A.利用Si和O在周期表中的位置
B.SiO2与水不发生反应
C.Si在一定条件下与氧气反应,生成SiO2
D.H2SiO3的酸性比H2O的酸性强
3、填空题 硅是重要的半导体材料,构成了现代电子工业的基础。回答下列问题:
(1)基态Si原子中,电子占据的最高能层符号?,该能层具有的原子轨道数为?、电子数为?。
(2)硅主要以硅酸盐、?等化合物的形式存在于地壳中。
(3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以?相结合,其晶胞中共有8个原子,其中在面心位置贡献?个原子。
(4)单质硅可通过甲硅烷(SiH4)分解反应来制备。工业上采用Mg2Si和NH4CI在液氨介质中反应制得SiH4,该反应的化学方程式为?。
(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
化学键
| C-C
| C-H
| C-O
| Si-Si
| Si-H
| Si-O
|
键能(KJ/mol)
| 356
| 413
| 336
| 226
| 318
| 452
|
①硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是?。
②SiH4的稳定性小于CH4,更易生成氧化物,原因是?。
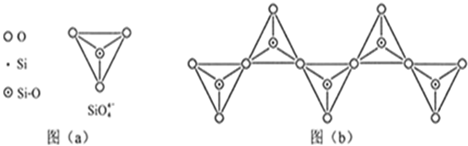
(6)在硅酸盐中,SiO44-四面体(如下图a)通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图b为一种无限长单链结构的多硅酸根;其中Si原子的杂化形式为?。Si与O的原子数之比为?化学式为?。
4、选择题 诺贝尔物理学奖曾授予“光纤之父”英国华裔科学家高锟以及两位美国科学家威拉德・博伊尔和乔治・史密斯。光导纤维的主要成分是二氧化硅,下列关于二氧化硅的说法正确的是
A.二氧化硅是酸性氧化物,因此能与水反应生成硅酸
B.用二氧化硅制取单质硅时,当生成2.24 L气体(标准状况)时,得到2.8 g硅
C.二氧化硅制成的光导纤维,由于导电能力强而被用于制造光缆
D.二氧化硅不能与碳酸钠溶液反应,但能与碳酸钠固体在高温时发生反应
5、选择题 地壳中含量第一和第二的两种元素形成的化合物,不具有的性质是
A.熔点很高
B.与水反应生成对应的酸
C.可与生石灰反应
D.与碳在高温下反应可制取两元素中的一种单质