1、实验题 某研究学习小组拟取盐湖苦卤的浓缩液(富含K+、Mg2+、Br-、SO42- 、Cl-等)来制取较纯净的氯化钾晶体及液溴,他们设计了如下流程:?

回答以下问题:
(1)操作I的名称:_________;要从橙色液体中分离出溴,所采取的操作需要的主要玻璃仪器除酒精灯和温度计外,还需要____________。
(2)试剂Z的化学式为_________;检验SO42-已除尽的方法是__________
(3)写出操作Ⅲ的具体操作步骤:___________
(4)某同学用如图所示的实验装置制取氧化剂并将其通入盐湖苦卤中。
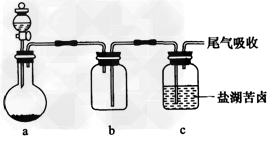
装置b在实验中的作用是________;若把上述装置中的a、b作为气体的发生、收集装置,装置c可 ?任意改进,则根据下列提供的药品,用这套装置还可以制取的气体是__________。?
①制NH3:浓氨水和碱石灰?
②制SO2:Cu片和浓硫酸 ?
③制NO:Cu片和稀硝酸?
④制O2:MnO2和双氧水
若用上述装置中的a、b制取并收集NO,应将装置b如何改进:____。
2、实验题 aF是一种重要的氟盐,主要用作农作物杀虫剂、木材防腐剂等。某课题组设计了以氟硅酸(H2SiF6)等物质为原料制取氟化钠,并得到副产品氯化铵的实验,其工艺流程如下:
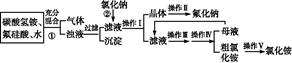
已知:20 ℃时氯化铵的溶解度为37.2 g,氟化钠的溶解度为4 g,Na2SiF6微溶于水。
(1)操作Ⅱ是洗涤、干燥,其目的是 ?,
操作Ⅲ和操作Ⅳ的名称依次是 (填写序号)。
a.过滤?b.加热蒸发? c.冷却结晶? d.洗涤
(2)上述流程中①的化学反应方程式:
H2SiF6+ NH4HCO3 NH4F+? H2SiO3↓+ CO2↑+ ?
NH4F+? H2SiO3↓+ CO2↑+ ?
(3)流程①中NH4HCO3必须过量,其原因是? 。
(4)若不考虑氟化钠的溶解,7.2 g氟硅酸理论上最多能生产 g氟化钠。
3、选择题 海带中含碘元素,从海带中提取碘有如下步骤:①通入足量Cl2 ?②将海带焙烧成灰后加水搅拌?③加CCl4振荡?④用分液漏斗分液?⑤过滤
合理的操作顺序是(? )
A.①②③④⑤
B.②⑤①③④
C.①③⑤②④
D.②①③⑤④
4、选择题 海水中含有的氯化镁是镁的重要来源之一。从海水中制取镁有多种生产方法,可按如下步骤进行:①把贝壳制成石灰乳?②在引入的海水中加石灰乳,沉降、过滤、洗涤沉淀物?③将沉淀物与盐酸反应,结晶、过滤、干燥产物?④将得到的产物熔融后电解
关于从海水中提取镁的下列说法不正确的是(? )
A.此法的优点之一是原料来源丰富
B.进行①②③步骤的目的是从海水中提取氯化镁
C.第④步电解制镁是由于镁是很活泼的金属
D.以上制取镁的过程中涉及的反应有分解反应、化合反应和置换反应
5、选择题 现 有两组混合液:①乙酸乙酯和乙酸钠溶液?②乙醇和丁醇,分离以上各混合液的正确方法依次是?(?)
有两组混合液:①乙酸乙酯和乙酸钠溶液?②乙醇和丁醇,分离以上各混合液的正确方法依次是?(?)
A.分液、萃取
B.萃取、蒸馏
C.分液、蒸馏
D.蒸馏、萃取