1、选择题 在0.1 mol・L-1Na2CO3溶液中,下列关系正确的是?(?)
A.c(Na+)>c(CO32一)>c(OH一)>c(HCO3一)>c(H+)
B.c(Na+)+c(H+)=c(HCO3一)+c(CO32-)+c(OH一)
C.c(Na+)>c(CO32一)>c(HCO3-)>c(H+)>c(OH一)
D.c(HCO3一)+2c(CO32一)+c(H2CO3)="0.1" mol・L-1
2、填空题 (9分)已知25℃时,CH3COOH和NH3・H2O的电离平衡常数分别为Ka(CH3COOH)=l.7×10-5mol/L,Kb(NH3・H2O)=1.7×l0-5mol/L。现有常温下1 mol/L的醋酸溶液和l mol/L的氨水,且知醋酸溶液的pH=a,试回答下列问题:
(1)醋酸溶液中存在的电离平衡用电离方程式表示为?,
(2)将上述两种溶液等体积混合,所得溶液的pH=?。
(3)饱和氯化铵溶液显酸性,原因是(用离子方程式表示)?;向饱和氯化铵溶液中加入少量Mg(OH)2固体,固体完全溶解。甲、乙两位同学分别提出了不同的解释:
甲同学:由于NH4+水解呈酸性,其H+结合Mg(OH)2电离的OH-,使Mg(OH)2溶解
乙同学:由于Mg(OH)2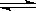 Mg2++2OH-,NH4++OH-
Mg2++2OH-,NH4++OH-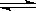 NH3・H2O,使Mg(OH)2溶解。请你设计一个实验验证两位同学的解释?。
NH3・H2O,使Mg(OH)2溶解。请你设计一个实验验证两位同学的解释?。
3、选择题 为了除去MgCl2溶液中的Fe3+,可在加热搅拌的条件下加入的一种试剂是
A.NaOH
B.Na2CO3
C.氨水
D.MgO
4、选择题 常温下,下列溶液中的微粒浓度关系正确的是( )
A.新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-)
B.pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
C.常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)=c(NH4+)>c(OH-)=c(H+)
D.0.1 mol・L-1CH3COONa溶液中:c(OH-)=c(CH3COOH)+c(H+)
5、选择题 常温下测得NaA盐溶液的PH值是10,有关盐NaA的说法正确的是?(?)
A.强酸弱碱盐
B.强碱弱酸盐
C.强酸强碱盐
D.弱酸弱碱盐