1、填空题 有A、B、C、D、E五种短周期元素,其中A、B、C三元素在元素周期表中的位置如图所示,已知A、C两种元素的质子数之和等于B的质子数,B、D、E属于同一周期,D元素原子的最外层只有一个电子,E元素的质子比D元素的质子数多两个。据此填空

(1)A在元素周期表中的位置为_________________, A、B、C、D、E的单质中,氧化性最强的是
___________(写化学式)。
(2)A的氢化物的结构式为___________,属于___________(填“共价”或“离子”)化合物。
(3)C的氢化物的电子式为___________,由电子式表示D和B所形成的化合物的过程_______________。
(4)E的氧化物与D的最高价氧化物对应的水化物反应的离子方程式为______________________。
参考答案:(1)第二周期、第VA族;F2
(2) ;共价
;共价
(3)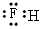 ;
;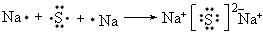
(4)2OH-+Al2O3==2AlO2-+H2O
本题解析:
本题难度:一般
2、选择题 关于元素周期表的说法正确的是
[? ]
A.元素周期表有8个主族
B.元素周期表有7个周期
C.短周期是指第一、二周期
D.IA族的元素全部是金属元素
参考答案:B
本题解析:
本题难度:简单
3、填空题 原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。
(1)X元素是________。
(2)X与W组成的化合物中存在________键(填“离子”或“共价”)。
(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为_______________________。
(4)由X、Y、Z、W四种元素组成的一种离子化合物A
①已知1?mol?A能与足量NaOH浓溶液反应生成标准状况下44.8?L气体。写出加热条件下A与NaOH溶液反应的离子方程式_________________________。
②又知A既能与盐酸反应,又能与氯水反应,写出A与氯水反应的离子方程式____________________________。
(5)由X、Y、Z、W和Fe五种元素组成的式量为392的化合物B,1?mol?B中含有6?mol结晶水。对化合物B进行如下实验:a取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时间白色沉淀变为灰?绿色,最终变为红褐色; b另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解
①B的化学式为____________?。
②已知1?mol/L?100?mL?B溶液能与1?mol/L?20?mLKMnO4溶液(硫酸酸化)恰好反应。写出反应的离子方程式__________________________。
参考答案:(1)H
(2)共价
(3)3Cu+2NO3-+8H+===3Cu2++2NO↑+4H2O
(4)①NH4++OH-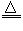 H2O+NH3↑;②SO32-+Cl2+H2O===SO42-+2Cl-+2H+
H2O+NH3↑;②SO32-+Cl2+H2O===SO42-+2Cl-+2H+
(5)①(NH4)2Fe(SO4)2・6H2O;②5Fe2++MnO4-+8H+===5Fe3++Mn2++4H2O
本题解析:
本题难度:一般
4、推断题 (三选一)【物质结构与性质】
已知:A、B、C、D为周期表1~36号中的元素,它们的原子序数逐渐增大。A的基态原子有3个不同的能级,各能级中电子数相等;C的基态原子2p能级上的未成对电子数与A原子相同;D的基态原子的M电子层上有4个未成对电子。
请回答下列问题:
(1)D是元素周期表中第____周期,第_______族的元素;其基态原子的外围电子排布式为____________________。
(2)A、B、C、D四种元素中,电负性最大的是________(填元素符号)。
(3)由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-中A原子的杂化方式为____________。B的氢化物的沸点远高于A的氢化物的主要原因是___________________。
(4)D能与AC分子形成D(AC)5,其原因是AC分子中含有________。D(AC)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断D(AC)5晶体属于_________(填晶体类型)。
(5)SiO2的晶胞可作如下推导:先将NaCl晶胞中的所有Cl-去掉,并将Na+全部换成Si原子,再在每两个不共面的“小立方体”中心处各放置一个Si原子便构成了晶体Si的一个晶胞。再在每两个相邻的Si原子(距离最近的两个Si原子)中心联线的中点处增添一个O原子,便构成了SiO2晶胞,故SiO2晶胞中有_______个Si原子,______个O原子。
参考答案:(1)四;?Ⅷ;3d64s2?
(2)O?
(3)sp;NH3分子间能形成氢键
(4)?孤对电子、分子晶体
(5)8;16
本题解析:
本题难度:一般
5、选择题 下列递变规律中,错误的是( )
A.Na、Mg、Al的还原性依次减弱
B.N2、O2、F2的氧化性依次增强
C.C、N、O的原子半径依次增大
D.P、S、Cl的最高化合价依次升高
参考答案:C
本题解析:
本题难度:一般