|
���л�ѧ֪ʶ����ɡ�Ӱ�컯ѧ��Ӧ���ʵ����ء����߲��ԣ�2019�����°棩(��)
2020-07-28 03:53:02
�� �� �� ��
|
1��ѡ���� ��������£���Ӧ������ͬ���� �� ��
A�������0.1 mol/L HCl��0.1 mol/L H2SO4�ֱ���0.2 mol/L NaOH��Һ��Ӧ
B��������п����п�۷ֱ������1 mol/L HCl��Ӧ
C���������Ũ��HCl��HNO3�ֱ����������Na2CO3��ĩ��Ӧ
D�������0.2 mol/L HCl��0.1 mol/L H2SO4������ȱ������Ʒ��ʯ��ʯ��Ӧ
|
�ο��𰸣�C
��������������0.1 mol/L HCl��0.1 mol/L H2SO4�ֱ���0.2 mol/L NaOH��Һ��Ӧ������������Ũ����Ȼ��ͬ����[H+]��ͬ����ѧ��Ӧ���ʲ�ͬ��A��������п����п�ۣ����ǵĽӴ������ͬ����ѧ��Ӧ���ʲ�ͬ��B���������Ũ��HCl��HNO3�ֱ����������Na2CO3��ĩ��Ӧ�����ǵ�H+��Ũ����ͬ����ѧ��Ӧ������ͬ��C��ȷ�������0.2 mol/L HCl��0.1 mol/L H2SO4������ȱ������Ʒ��ʯ��ʯ��Ӧ��������ʯ��ʯ��Ӧ���������ܣ�������ʯ��ʯ���棬��ֹ��Ӧ�Ľ��У����ʼ�������ֹͣ��D����
���㣺����Ӱ�컯ѧ��Ӧ���ʴ�С�����ء�
�����Ѷȣ�һ��
2��ѡ���� �����оٵĸ�����ʵ�д��������ϵ����
[? ]
����I��ԭ��
���������
A.
O3������������
�������е�O3����Ϊ����ɡ
B.
��ԭ�Ӻ��������������
�ƵĽ����Ա���ǿ
C.
��������Ա�������ǿ
��Ԫ�صķǽ����Ի�̼Ԫ��ǿ
D.
N2+3H2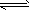 2NH3�Ƿ��ȷ�Ӧ 2NH3�Ƿ��ȷ�Ӧ
��ҵ�ϳɰ��ķ�Ӧ�ڸ����½���
�ο��𰸣�A
���������
�����Ѷȣ�һ��
3������� ijѧ����0��1��10��25�L3������������99��5%����Ƭ���ᷴӦ��ȡH2��ʵ��������±�

��1��д����Ƭ���ᷴӦ�����ӷ���ʽ________________________��
��2����Ӧ1-15min�ڣ���������ķ�Ӧ�����ӿ죬��ԭ����_____________________________��
��3��������Ƭ����������ᷴӦ����IJ��죬����˼�������������²��룺
����һ��____________________________________��
�������____________________________________��
�ο��𰸣���1��2Al+6H+==2Al3++3H2��
��2����Ӧ�����¶����ߣ���ѧ��Ӧ���ʼӿ�
��3������һ��Cl-�Ը÷�Ӧ�дٽ�����
�������SO42-�Ը÷�Ӧ����������
���������
�����Ѷȣ�һ��
4������� (1)�������С���Ѿ������˻�ѧ��Ӧ�ķ�Ӧ���д�������Ļ�ѧ��Ӧ����ʽ����ƽ����ÿС��2�֣���6�֣�
������������͵�������Ӧ
����ˮ�⣺
CH3CH(OH)CH3�Ĵ�������
(2)��4�֣�.��-��ѭ���ֽ�ˮ������Ҫ�漰���з�Ӧ��
��.SO2+2H2O+I2===H2SO4+2HI ��.2HI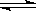 H2+I2 ��.2H2SO4===2SO2+O2+2H2O H2+I2 ��.2H2SO4===2SO2+O2+2H2O
��1��һ���¶��£���1L�ܱ������м���1mol HI��g����������Ӧ�����ɵ�I2Ϊ���壬H2���ʵ�����ʱ��ı仯��ͼ��ʾ��0-2 min�ڵ�ƽ����Ӧ���ʦԣ�HI��=
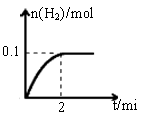
��2��ʵ������Zn��������ȡH2��Ϊ�˼ӿ췴Ӧ���ʣ����д�ʩ�����е��� ������ţ�
a������Ũ���� b����������CuSO4���� c���ô�п���洿п
d������ e.��п��Ū��п�� f.��98.3%Ũ����
�ο��𰸣�(1)��ÿС��3�֣���6�֣�
3CH3COOH��CH2OHCHOHCH2OH  ��3H2O ��3H2O

2CH3CHOHCH3��O2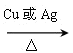 2CH3COCH3��2H2O 2CH3COCH3��2H2O
(2)�����֣���1��0.1mol/(L��min)---2��, ��2��a��f--2��
�����������1�������к���3���ǻ������Ժ����ᷢ��������Ӧ������3�������ᡣ�����Ƕ��ǣ�ˮ�����������Ǻ��ǡ�2�������к��ǻ�������̼ԭ����ֻ��1����ԭ�ӣ��������IJ����DZ�ͪ��
��2������ͼ���֪��ƽ��ʱ���������ʵ�����0.1mol���������ĵ⻯����0.2mol������䷴Ӧ������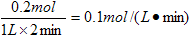 �� ��
��3��������������Է�Ӧ���ʵ�Ӱ�졣Ũ�����Ũ���ᶼ���������ᣬ��п��Ӧ�����ﲻ��������b��c�п��Թ���ԭ��أ���Ӧ���ʿ��Լӿ졣�¶����ߣ���Ӧ���ʼӿ졣e������Ӧ��ĽӴ��������Ӧ���ʼӿ졣���Դ�ѡaf��
�����Ѷȣ�һ��
5��ѡ���� ��������������ʢ��һ�������ϡ������Թ��У���ʹ��Ӧ���ʽ����Ҳ�Ӱ��H2�������IJ�����
A����������FeCl3��Һ
B����������KNO3��Һ
C������������K2CO3��Һ
D����������Na2SO4��Һ
�ο��𰸣�D
����������Ȼ���ˮ�⣬��Һ�����ԣ��������ɵ����������ӣ�A����ȷ�������������£�����ؾ���ǿ�����ԣ��ͽ�����Ӧ�ò���������B����ȷ��C�е�̼��ؿ������������ӣ����ͷ�Ӧ���ʣ������ɵ����������٣�����ȷ����������Һ�൱����ϡ�ͣ���Ӧ���ʽ��ͣ������ɵ����������䣬��ѡD��
���㣺������������Է�Ӧ���ʵ�Ӱ��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣�����ۺ���ǿ�����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ����ּ�ڿ���ѧ��������û���֪ʶ���ʵ�����������������Ĺؼ���Ҫ��ȷ������������Ӱ�췴Ӧ���ʵģ�Ȼ��������������ü��ɣ�����������ѧ����Ӧ��������������������
�����Ѷȣ�һ��
|