| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点大全《电解池原理》在线测试(2019年最新版)(二)
参考答案:A 本题解析:从电流的流向可以判断a是正极,b是负极,A.电解过程中,d电极接电源的负极做阴极,发生反应为:Cu2+ + 2e- =Cu,质量增加,对;B.d电极接电源的负极做阴极,不是阳极,错;C.a为正极、b为负极,错;D.电解过程中,氯离子在阳极放电,发生2Cl? - 2e- = Cl2↑浓度减小,错,选A。 本题难度:一般 3、选择题 用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入 0.1molCu(OH)2后恰好恢复到电解前的浓度和PH。则电解过程中转移的电子数为( ) |
参考答案:D
本题解析:根据电解池的工作原理,要想让电解后的电解质复原,则遵循的原则是:出什么加什么,加入 Cu(OH)2后溶液与电解前相同,则铜离子和氢氧根放电。
Cu(OH)2从组成上可看成CuO?H2O,溶液中加入0.1 mol Cu(OH)2后,溶液恰好恢复到电解前的浓度和pH,这说明电解生成了0.1 mol 氧化铜,并消耗0.1 mol H2O。由电解的总反应式可知:
2H2O+2CuSO4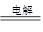 2Cu+O2↑+2H2SO4 转移电子
2Cu+O2↑+2H2SO4 转移电子
2mol 4mol
0.1mol 0.2mol
2H2O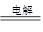 2H2↑+O2↑ 转移电子
2H2↑+O2↑ 转移电子
2mol 4mol
0.1mol 0.2mol
所以电解过程中共转移电子为0.2mol+0.2mol=0.4 mol,答案选D。
考点:考查电解的有关计算
点评:该题是高考中的常见题型,属于中等难度试题的考查。试题综合性强,贴近高考,有利于激发学生的学习兴趣和学习积极性。明确电解池的工作原理,先根据原子守恒计算析出铜单质的物质的量,再根据铜与转移电子之间的关系计算转移电子的物质的量。该题的关键是准确判断出电解分为2个阶段。
本题难度:一般
4、选择题 在1 LK2SO4和CuSO4的混合溶液中,c(SO42-)=2.0 mol・L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4 L(标况)气体,则原溶液中K+的物质的量浓度为?(?)
A.2.0 mol・L-1
B.1.5 mol・L-1
C.1.0mol・L-1
D.0.5 mol・L-1
参考答案:A
本题解析:略
本题难度:一般
5、填空题 如图为相互串联的甲乙两电解池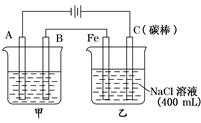
试回答:
(1)甲池若为用电解原理精炼铜的装置,则A是 极,材料是 ,
电极反应为 。
(2)乙池中若滴入少量酚酞试液,电解一段时间后Fe极附近呈 色.
(3)若甲池为电解精炼铜,阴极增重12.8g,则:乙池中阳极放出的气体在标准状况下的体积为
;若此时乙池剩余液体为400 mL,则电解后得到碱液的物质的量浓度为 。
参考答案:1)阴极;纯铜;Cu2++2 e- =" Cu" ;(2)红;
(3)4.48L;1mol/L
本题解析:结合装置图,与电源负极相连的是阴极,与电源正极相连的是阳极,甲池若为用电解原理精炼铜的装置,则A是阴极,材料为纯铜,发生电极反应是Cu2++2 e- = Cu。
乙池中实质是电解NaCl饱和溶液,C极上放出Cl2,Fe极上生成H2 ,2H2O+2e-=H2↑+2OH,若滴入少量酚酞试液,电解一段时间后Fe极附近呈红色。若甲池为电解精炼铜,阴极增重12.8g,即转移的电子有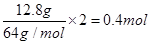 ,则乙池中阳极放出的气体在标准状况下的体积为
,则乙池中阳极放出的气体在标准状况下的体积为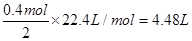 ;产生OH-有0.4mol,若此时乙池剩余液体为400 mL,则电解后得到碱液的物质的量浓度为
;产生OH-有0.4mol,若此时乙池剩余液体为400 mL,则电解后得到碱液的物质的量浓度为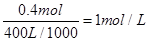 。
。
考点:电解池
点评:考查电解池实验装置图,难度不大,解题的关键是要区分正负极,电极发生的反应,把握得失电子情况,仔细计算。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点总结《原子的结构.. | |