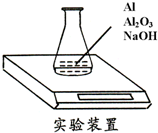
1、简答题 某种由Al与Al2O3粉末组成的混合物样品,利用如图装置测定混合物中Al的质量分数(已知样品质量为2.58g、锥形瓶和过量NaOH溶液的总质量为185.72g),每隔相同时间读得电子天平的数据如表:
读数次数
质量(g)
|
锥形瓶
+
NaOH溶液
+
试样
第1次
188.30
第2次
188.28
第3次
188.25
第4次
188.24
第5次
188.24
|
(1)Al与NaOH溶液反应的化学方程式为______.
(2)反应中产生的氢气质量为______g
(3)求样品中Al的质量分数.______(要求有计算过程).
参考答案:(1)铝和氢氧化钠反应生成偏铝酸钠和氢气,反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(2)称量至恒重是需要的数据,依据图表数据可知,称重恒重的质量为188.24g,所以反应产生的氢气质量为188.30-188.24=0.06g
(3)依据反应可知,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,生成氢气0.03mol,需要铝物质的量为0.02mol;
样品中Al的质量为0.02mol×27=0.541g;则样品中Al的质量分数为0.54g2.58g×100%=20.9%;
故答案为:生成氢气0.03mol,需要铝物质的量为0.02mol;样品中Al的质量为0.02mol×27=0.541g;则样品中Al的质量分数为0.54g2.58g×100%=20.9%;
本题解析:
本题难度:一般
2、选择题 可以用来鉴别0.1mol/L的Na2S、NaI、Na2CO3、NaAlO2、Na2SO4五种溶液的是( )
A.烧碱溶液
B.氯化钡溶液
C.氨水
D.硫酸铁溶液
参考答案:D
本题解析:
本题难度:一般
3、选择题 下列所示的实验装置能达到实验目的的是
[? ]
A.制取氨气 
B.测定化学反应速率 
C.稀释浓硫酸 
D.比较KMnO4、Cl2、S的氧化性 
参考答案:D
本题解析:
本题难度:一般
4、实验题 据下图提供的仪器装置,完成提纯并测定Na2 CO3 样品的纯度(其中含NaHCO3杂质)。

请回答下列问题:
实验一
测定Na2CO3样品中NaHCO3分解放出的CO2 的体积。
(1)连接装置的正确顺序是___。
(2)完成实验一尚缺少的仪器是___。
(3)产生的气体从装置④的___端进入。
(4)实验二
测定经实验一后的固体物质与盐酸反应放出的CO2的体积,应将实验一的装置做哪些调整?____ 。
(5)实验一不再产生气体时,通过量筒内的水位读数折算成标准状况下产生aL CO2,实验二中加盐酸无气体产生时,通过量筒内水位读数折算成标准状况下产生bLCO2。则该样品中Na2CO3纯度的实验值为___。
(6)如果实验二用浓盐酸作试剂,对最终的实验结果可能会产生怎样的影响?_____________
参考答案:(1)⑥①③④⑤
(2)酒精灯
(3)a
(4)将③换成②,并将试管直立,撤走酒精灯
(5)[53(b-a)÷(53b+ 31a)]×100%
(6)使测定的碳酸钠的纯度偏高
本题解析:
本题难度:一般
5、简答题 如图所示,A、B、C是实验室常用的三种制取气体的装置,提供的药品有:大理石、浓盐酸、稀盐酸、锌粒、二氧化锰、氯化铵、熟石灰.现利用这些药品分别制取NH3、Cl2、H2、CO2四种气体,试回答以下问题.
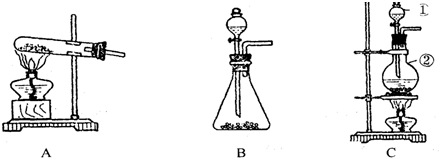
(1)选用A装置可制取的气体有______选用C装置制取的气体有______.
(2)标号①、②的仪器名称依次为______.
(3)写出利用上述有关药品制取氨气的化学方程式:______.
若要制得干燥的氨气,可选用下列干燥剂中的______(填序号).
a.生石灰?b.浓硫酸?c.碱石灰?d.五氧化二磷.
参考答案:(1)A装置中反应物的状态是固体.反应条件是加热,所以可制取氨气;C装置的反应物状态是固体、液体混合态,反应条件是加热,所以可制取氯气.
故答案为:NH3,Cl2.
(2)a是分液漏斗,b是圆底烧瓶.
故答案为:分液漏斗,圆底烧瓶.
(3)氯化铵和氢氧化钙反应生成氨气、水和氯化钙,反应条件是加热.
故答案为:Ca(OH)2+2?NH4Cl?△?.?2?NH3↑+2H2O+CaCl2?
(4)氨气是碱性气体,所以不能用酸作干燥剂,可用碱性物质或中性物质作干燥剂.
故选a?c.
本题解析:
本题难度:一般