1������� ʵ��������240ml?0.2mol?L-1��Na2CO3��Һ���ش��������⣺
��1��Ӧ��������ƽ��ȡNa2CO3?10H2O����______?g��
��2������ʱӦ��ѡ��������ƽ��ҩ�ס��ձ�������������ͷ�ι��⣬����Ҫ�õ���������______��
��3������ƿ�ϱ��У����¶ȡ���Ũ�ȡ�����������ѹǿ���ݿ̶��ߡ�����ʽ���ʽ�������е�______��������ţ�
��4������ʱ��һ��ɷ�Ϊ���¼������裺�ٳ���?�ڼ���?���ܽ�?��ҡ��?��ת��?��ϴ��?�߶���?����ȴ������ȷ�IJ���˳��Ϊ______��
��5����ʵ��ʱ���������������ʹ��Һ��Ũ��ƫ�͵���______������ѡ��
A�����ǽ�ϴ��Һת������ƿ��
B������ƿϴ�Ӻ��ڱ���ˮ���δ�����ﴦ����
C�����ݡ�ҡ�ȡ����ú��ְ�����ڿ̶����ּ�ˮ���̶��ߣ�
D������ʱ���ӿ̶��ߣ�
E��Na2CO3?10H2O��ʧȥ���ֽᾧˮ��
�ο��𰸣���1����������Һ�����Ϊ240ml��������ƿ�Ĺ��û��240ml��ֻ��ѡ��250ml��Na2CO3�����ʵ���n=cV=0.25L��0.2mol?L-1=0.05mol��Na2CO3?10H2O�����ʵ�������Na2CO3�����ʵ���������Na2CO3?10H2O������0.05mol��286g/mol=14.3g���ʴ�Ϊ��14.3��
��2�����Ʋ����м��㡢�������ܽ⡢��ȴ����Һ��ϴ�ӡ����ݡ�ҡ�ȵȲ�����һ����������ƽ��������ҩ��ȡ��ҩƷ�����ձ����ܽ⣬��ȴ��ת�Ƶ�250mL����ƿ�У����ò���������������ˮ��Һ�����̶���1��2cmʱ�����ý�ͷ�ιܵμӣ�������Ҫ������Ϊ��������ƽ��ҩ�ס��ձ�����������250mL����ƿ����ͷ�ιܣ��ʴ�Ϊ��250mL����ƿ��
��3��������ƿ�ϱ����¶ȡ��������̶��ߣ���ѡ���٢ۢݣ�
��4�����Ʋ����м��㡢�������ܽ⡢��ȴ����Һ��ϴ�ӡ����ݡ�ҡ�ȵȲ������ʴ�Ϊ���ڢ٢ۢ�ݢޢߢܣ�
��5��A�����ǽ�ϴ��Һת������ƿ�����ʵ�����ƫС��Ũ��ƫС����A��ȷ��
B������ƿϴ�Ӻ��ڱ���ˮ���δ�����ﴦ������Һ��������䣬Ũ�Ȳ��䣬��B����
C�����ݡ�ҡ�ȡ����ú��ְ�����ڿ̶����ּ�ˮ���̶��ߣ���Һ�����ƫ��Ũ��ƫС����C��ȷ��
D������ʱ���ӿ̶��ߣ���Һ�����ƫС��Ũ��ƫ��C����
E��Na2CO3?10H2O��ʧȥ���ֽᾧˮ�����ʵ�����ƫ��Ũ��ƫ��E����
�ʴ�Ϊ��A��C��
���������
�����Ѷȣ�һ��
2��ѡ���� ��100 mL NaOH��Һ��ͨ��һ������CO2���壬��ַ�Ӧ������������Һ����μ���0.2 mol/L�����ᣬ����CO2������������������֮���ϵ����ͼ��ʾ�������ж���ȷ����
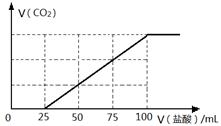
A��ԭNaOH��Һ��Ũ��Ϊ0.1 mol/L
B��ͨ��CO2�����Ϊ448 mL
C��������Һ�����ʳɷֵ����ʵ���֮��Ϊn(NaOH)��n(Na2CO3) =" 1:" 3
D��������Һ�����ʳɷֵ����ʵ���֮��Ϊn(NaHCO3)��n(Na2CO3) =" 2:" 1
�ο��𰸣�D
�����������0��25mLû���������ɣ���25mL��ʼ���������ɶ�����̼���壬����������100mL��25mL=75mL�������������ĵ���������Ϊ1��3����NaOH��Һͨ��һ����CO2��Ӧ����Һ�е��������ʵ����Ĺ�ϵ��Na2CO3��NaHCO3=1��2��D��ȷ����C������HCl��NaCl��NaOH����NaOH�����ʵ���Ϊ0.1L��0.2mol/L=0.02mol��Na+�����ʵ���Ũ��Ϊ0.02/0.1=0.2mol/L����A������Na2CO3��NaHCO3=1��2����̼ԭ���غ��֪������̼�����ʵ���Ϊ0.075*0.2=0.015mol������������������CO2��������ڱ�״����Ϊ0.015mol��22.4L/mol=336mL��B����
�����Ѷȣ�һ��
3��ѡ���� ��1 L 1 mol��LNaOH��Һ��ȡ��100 ml�����й�����100 ml��Һ�������д������
A����NaOH 0.1 mol
B��Ũ��Ϊ1 mol��L
C����NaOH 4g
D��Ũ��Ϊ0.1 mol��L