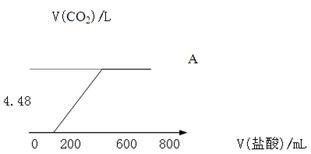
1、填空题 向NaOH溶液中通入CO2气体,充分反应后,在所得溶液中逐滴加入1mol/L的盐酸,所加盐酸体积(mL)与产生CO2气体的体积(L)的关系如图所示。
试填写下列空白:
V(CO2)/L
(1)与盐酸反应前,A溶液中的溶质是 。
(2)其物质的量之比是 。
参考答案:(4分)(1)Na2CO3、 NaHCO3 (2) 1:1
本题解析:(1)根据图像可知,开始加入盐酸时并没有立即生成CO2气体,其中生成CO2消耗的盐酸是前面的2倍。由于碳酸钠和盐酸反应是分步进行的,首先生成碳酸氢钠,然后碳酸氢钠再和盐酸反应生成CO2,所以与盐酸反应前,A溶液中的溶质是Na2CO3、NaHCO3。
(2)根据反应的方程式Na2CO3+HCl=NaCl+NaHCO3、NaHCO3+HCl=NaCl+H2O+CO2↑可知,由于生成CO2消耗的盐酸是前面的2倍,所以二者的物质的量之比应该是1
本题难度:困难
2、选择题 某晶体的相对分子质量为250,取该晶体12.5g加热,使其失去全部结晶水后,称其质量为8g,则该晶体中结晶水的个数为( )
A.2
B.5
C.7
D.10
参考答案:根据题意可知,晶体的物质的量n=mM=12.5g250g/mol=0.05mol,晶体中结晶水的质量=12.5g-8g=4.5g,所以结晶水的物质的量为:4.5g18g/mol=0.25mol,故结晶水合物中结晶水的个数=0.25mol0.05mol=5.
故选B.
本题解析:
本题难度:一般
3、选择题 在T℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g・cm-3,溶质的质量分数为w,其中含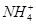 的物质的量为b mol。下列叙述中正确的是( )
的物质的量为b mol。下列叙述中正确的是( )
A.溶质的质量分数为w=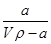 ×100%
×100%
B.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w
C.溶液中c(OH-)=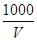 mol・L-1
mol・L-1
D.溶质的物质的量浓度c=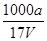 mol・L-1
mol・L-1
参考答案:D
本题解析:溶液的质量是Vρg,所以溶质的质量分数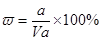 ,A不正确;氨水的密度小于水的,所以上述溶液中再加入V mL水后,所得溶液溶质的质量分数小于0.5w,B不正确;溶液中OH-的物质的量大于bmol,浓度大于
,A不正确;氨水的密度小于水的,所以上述溶液中再加入V mL水后,所得溶液溶质的质量分数小于0.5w,B不正确;溶液中OH-的物质的量大于bmol,浓度大于 ,所以选项C不正确;溶质氨气的物质的量是a/17mol,所以溶液的浓度是c=
,所以选项C不正确;溶质氨气的物质的量是a/17mol,所以溶液的浓度是c=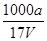 ?mol・L-1,D正确,答案选D。
?mol・L-1,D正确,答案选D。
本题难度:一般
4、选择题 下列说法正确的是( )。
A.标准状况下,11.2 L乙醇完全燃烧产生的CO2的分子数为NA
B.含1 mol H2SO4的浓硫酸与足量铜反应转移的电子数为NA
C.1 L 0.1 mol・L-1硅酸钠溶液中含有0.1NA个SiO32―
D.标准状况下,a L的氧气和氮气的混合物含有的原子总数为
参考答案:D
本题解析:A项,标准状况下乙醇是液体,故错误;B项,含1 mol H2SO4的浓硫酸与足量铜反应,浓硫酸不能完全反应,故转移的电子数小于NA,错误;C项,SiO32―会发生水解,故1 L 0.1 mol・L-1硅酸钠溶液中含有的SiO32―少于NA个,错误。
本题难度:一般
5、选择题 在1 L 1mol?L-1的氨水中( )
A.含1 mol NH3分子
B.含NH3、NH4+之和为1 mol
C.含1 mol NH3?H2O
D.含NH3、NH3?H2O、NH4+之和为1 mol
参考答案:D
本题解析:氨水是弱碱,部分电离,所以NH3和NH3・H2O物质的量均小于1mol,A、C错误;由氮元素守恒知NH3、NH3?H2O、NH4+之和为1 mol,D正确、B错误。
点评:NH3+H2O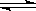 NH3・H2O
NH3・H2O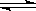 NH4++OH-
NH4++OH-
本题难度:一般