1��ѡ���� ����ʵ���У���������������ȫ�ܽ����
[? ]
A����H2O2��Һ�м�������MnO2��ĩ
B����п��Ƥ����������NaOH��Һ��
C��1molͭƬ�뺬2molH2SO4��Ũ���Ṳ��
D��������1molͭƬͶ�뺬4molHNO3��Ũ������
2������� ��ȸʯ��Ҫ��Cu2(OH)2CO3����������Fe��Si�Ļ�����Կ�ȸʯΪԭ�Ͽ��Ʊ�CuSO4��5H2O�����ײ���G����������ҳͼʾ����ش��������⣺

��1����ҺA�Ľ���������Cu2+��Fe2+��Fe3+�������������Լ���ѡ��ʵ�鲽���У��Լ������Ϊ
_______������ţ���������ҺA��Fe3+������Լ�Ϊ_______������ţ���
a��KMnO4 b��(NH4)2S c��H2O2 d��KSCN
����D�г��˹�����CuO�⣬��������һ�ֹ��壬�仯ѧʽΪ_______������CuO������______________��
��2������ҺC���CuSO4��5H2O����Ҫ����һϵ�в��������ձ���©���⣬���˲������õ���һ�����������������ڴ˲����е���Ҫ������_____________________��
��3���Ʊ����ײ���Gʱ��Ӧ��CaCl2��Һ����ͨ�루���ȼ��룩_______���ѧʽ����д���÷�Ӧ�Ļ�ѧ����ʽ_____________________��
��4�����ⶨ��ҺA��Fe2+��Ũ�ȣ�����KMnO4����Һ�ζ���ȡ��KMnO4����ҺӦ��______________����д�������ƣ���ȡA��Һϡ��һ����������KMnO4����Һ�ζ����յ�����Ϊ_________________
3������� CuSO4��Һ����ѧ��ѧ����ũҵ�����г�����һ���Լ���
��1��ijͬѧ����CuSO4��Һʱ����ʢ��һ��������ͭ������ձ��м�������������ˮ�������Ͻ��裬����õ�����Һ������Ϊ�ǹ���û����ȫ�ܽ⣬���Ƕ�����Һ���ȣ�������ֻ��Ǹ������ˣ�ԭ����_________________����������ձ��м�����һ������________��Һ���õ��˳����CuSO4��Һ��
��2����ͬѧ�����Ƶõ�CuSO4��Һ����������ʵ��̽����
�� ͼһ�Ǹ��ݷ�ӦZn + CuSO4 = Cu + ZnSO4��Ƴɵ�пͭԭ��ء�
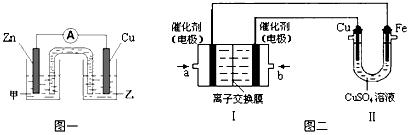
�������Һ����_________���ZnSO4����CuSO4������Һ��Cu���ĵ缫��Ӧʽ��________________��
��ͼ���У����Ǽ���ȼ�ϵ�أ��������ҺΪKOH��Һ���Ľṹʾ��ͼ����ͬѧ���ڢ���ʵ�����϶�ͭ����b��ͨ�����_________���CH4����O2������a���缫�Ϸ����ĵ缫��Ӧʽ��_________________��
��3����������CuSO4��5H2O������ʯ�Һ�ˮ��һ��������ϣ����ɵõ�������Һ��ɱ������������Ч�ɷ�Ϊ���ܵļ�ʽ����ͭ[xCuSO4��yCu(OH)2]��Ϊ�ⶨij��ʽ����ͭ����ɽ���������ʵ�飺ȡ�������ļ�ʽ����ͭ��Ʒ���ݣ�һ�ݵμ�ϡ������ǡ����ȫ�ܽ⣬��һ�ݸ������պ�ֻ�õ�CuO���塣����������ʾn(HCl)�Un(CuO)��3�U2����ü�ʽ����ͭ�Ļ�ѧʽ��x�Uy=_______________��
4������� ��Cu��ŨH2SO4��Ӧ�������ͨ��Ʒ����Һ�����Թ۲쵽____________��˵��������___________________���ѧʽ�����塣����������ͨ��Na2SiO3��Һ�У��ɹ۲쵽_________________��˵���ܲ����������ԭ��_____________________���������ּ������ɣ�
5��ѡ���� ��ȥͭ���л������������ͭ������Ҫ���������ǣ�������
A���ڿ�����ȼ��
B��������ϡ���ᡢ�ȡ�����
C��������ˮ���ȡ�����
D��������ϡ���ᡢ�ȡ�����