|
|
|
高考化学知识点总结《盐类水解的原理》试题预测(2019年最新版)(一)
2020-07-28 04:45:54
【 大 中 小】
|
1、填空题 (4分)物质的量浓度相同的 ① 氨水 ② 氯化铵 ③ 碳酸氢铵 ④ 硫酸氢铵 ⑤ 硫酸铵五种溶液中c(NH4+)大小的顺序是__________________,溶液pH大小的顺序是__________________。
2、选择题 现有1.0 mol/L的NaOH溶液0.1L,若通入标准状况下体积为2.24L 的SO2气体,使其充分反应后,则所得溶液中各粒子浓度大小关系正确的是
A.c(Na+)+c(H+) = c(HSO3
|
3、选择题 下列用来表示物质变化的化学用语中,正确的是
A.钢铁发生电化学腐蚀的正极反应式: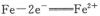
B.HS-的水解方程式:
C.CO32-的水解方程式:
D.AlCl3溶液与Na2CO3溶液混合:
|
4、选择题 加热蒸干并灼烧(低于400℃)下列物质的溶液,可以得到该固体物质的是
A.氯化铝
B.碳酸氢镁
C.碳酸钠
D.高锰酸钾
5、填空题 (16分)物质在水中可能存在电离平衡、盐的水解平衡等,它们都可看作化学平衡。请根据所学的知识回答:
(1)0.01mol/L的NH4Cl溶液中各种离子的浓度由大到小顺序为 ;电荷守恒关系: ;浓度为0.01mol/L的是 ; 和 两种粒子的浓度之和是0.01mol/L。
(2 )CH3COONa溶液中存在的2个平衡体系分别为(分别用离子方程式表示): 、 ;
(3) FeCl3溶液与Na2CO3溶液混合后,反应的离子方程式为 .