1、选择题 亚硝酸(HNO2)既可作氧化剂又可作还原剂,当它在反应中作氧化剂时,可能生成的产物是(? )
A.N2
B.N2O3
C.NH3
D.NO2
参考答案:AC
本题解析:亚硝酸中N呈现+3价,当它作氧化剂得电子,化合价要降低。N2中N呈0价,N2O3中N呈+3价,NH3中N呈-3价,NO2中N呈现+4价。故还原产物可能是N2或NH3。
本题难度:一般
2、简答题 已知化学能与其他形式的能可以相互转化.填写下表的空白:
| 化学反应方程式(例子) | 能量转化形式
①
由化学能转化为热能
②Pb+PbO2+2H2SO4

2PbSO4+2H2O
③CaCO3?CaO+CO2↑
参考答案:①可以通过燃烧将化学能转变为热能,如甲烷燃烧:CH4+2O2?点燃?.??CO2+2H2O,故答案为:CH4+2O2?点燃?.??CO2+2H2O
②铅蓄电池放电时将化学能转变为电能,充电时将电能转变为化学能,故答案为:化学能与电能之间的相互转化,
③高温分解CaCO3将热能转化为化学能,故答案为:热能转化为化学能.
本题解析:
本题难度:一般
3、实验题 用50 mL0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液,在如图所示的装置中进行中和反应。测定强酸与强碱反应的反应热。

?
| 起始温度t1/℃
| 终止温度
t2/℃
| 温度差
(t2-t1) /℃
| HCl
| NaOH
| 平均值
| 1
| 25.5
| 25.0
| 25.25
| 28.5
| 3.25
| 2
| 24.5
| 24.5
| 24.50
| 27.5
| 3.00
| 3
| 25.0
| 24.5
| 24.75
| 26.5
| 1.75
|
(1)在该实验中,量取50 mL 盐酸或NaOH 溶液,需要用到的玻璃仪器_________。
(2)装置中大、小烧杯之间填满碎泡沫塑料的目的是______________________________。
(3)某同学实验记录的数据如上表所示,其中记录的终止温度是指______________________________温度。
(4)计算该实验发生中和反应时放出的热量为________________kJ(中和后生成的溶液的比热容c=4.18J/(g・℃ )。
(5) 如果用50 mL 0.55mol/L的氨水(NH3・H2O)代替NaOH溶液进行上述实验,通过测得的反应热计算中和热,其中和热△H会偏大,其原因是
________________________?。
参考答案:(1)量筒、胶头滴管? (2)减少实验过程中的热量损失
(3)完全反应后混合溶液的最高温度? (4) 1.31 kJ?
(5) NH3・H2O是弱电解质,不能完全参加中和反应(或生成的盐会水解,要吸收热量等)
本题解析:(1)该实验量取盐酸或氢氧化钠溶液体积的玻璃仪器是量筒和胶头滴管。
(2)该实验过程中应该尽可能的减小热量的损失,所以装置中大、小烧杯之间填满碎泡沫塑料的目的是减少实验过程中的热量损失。
(3)根据实验原理可知,记录的终止温度是指完全反应后混合溶液的最高温度。
(4)根据表中数据可知,实验3的数据误差大,舍去。因此温度变化的平均值是(3.25℃+3.00℃)÷2=3.125℃。溶液的质量是100g,所以反应中放出的热量是4.18J/(g・℃ )×100g×3.125℃=1306.25J=1.31kJ。
(5)△H会偏大,说明反应中放出的热量减少。这是由于NH3・H2O是弱电解质,存在电离平衡,而电离是吸热的。
本题难度:一般
4、填空题 (10分)纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
方法Ⅰ
| 用炭粉在高温条件下还原CuO
| 方法Ⅱ
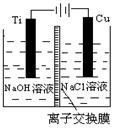
| 电解法,反应为2Cu + H2O 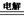 ?Cu2O + H2↑。 ?Cu2O + H2↑。
| 方法Ⅲ
| 用肼(N2H4)还原新制Cu(OH)2
|
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是? ▲?。
(2)已知:2Cu(s)+1/2O2(g)=Cu2O(s)? △H = -169kJ・mol-1
C(s)+1/2O2(g)="CO(g)?" △H = -110.5kJ・mol-1
Cu(s)+1/2O2(g)="CuO(s)?" △H = -157kJ・mol-1
则方法Ⅰ发生的反应:2CuO(s)+C(s)= Cu2O(s)+CO(g);△H =? ▲ ?kJ・mol-1。
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极反应式为?▲?。
(4)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放 出N2。该制法的化学方程式为? ▲?。 出N2。该制法的化学方程式为? ▲?。
(5)在相同的密闭容器中,用以上两种方法制得的Cu2O分别进行催化分解水的实验: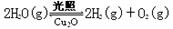 △H>0,水蒸气的浓度随时间t变化如下表所示。 △H>0,水蒸气的浓度随时间t变化如下表所示。

下列叙述正确的是? ▲?(填字母代号)。
A.实验的温度:T2<T1
B.实验①前20 min的平均反应速率v(H2)=7×10-5 mol・L-1 min―1 ?
C.实验②比实验①所用的催化剂催化效率高
参考答案:(每空2分,共10分)(1)反应不易控制,易还原产生Cu?
(2)+34.5?(3)2Cu-2e-+2OH-=Cu2O+H2O
(4)4Cu(OH)2 + N2H4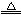 2Cu2O + N2↑ + 6H2O?(5)BC 2Cu2O + N2↑ + 6H2O?(5)BC
本题解析:略
本题难度:一般
5、选择题 对于反应:2X+Y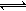 2Z(正反应为放热反应),若升高温度则能使( ) 2Z(正反应为放热反应),若升高温度则能使( )
A.反应速率不变,Z的产量减少
B.反应速率增大,Z的产量增大
C.反应速率增大,Y的转化率降低
D.反应速率减小,Z的产量增大
参考答案:C
本题解析:升高温度正逆反应速率都是增大,由于正方应是放热反应,所以平衡向逆反应方向移动,反应物的转化率降低,生成物的产量减少,答案选C。
点评:该题是高考中的常见题型和重要考点,属于中等难度试题的考查。试题基础性强,侧重对学生基础知识的巩固和训练,主要是考查学生对外界条件影响反应速率和平衡状态的熟悉了解程度,旨在考查学生灵活运用基础知识解决实际问题的能力。有利于培养学生的逻辑推理能力和发散思维能力。
本题难度:简单
|