1��ѡ���� ����˵�����ʾ������ȷ����(����)
A����Ӧ��������������������������ʱ��һ�������Է����з�Ӧ
B����֪��CH4(g)��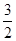 O2(g)=2H2O(l)��CO(g)����H����H��ʾCH4��ȼ����
O2(g)=2H2O(l)��CO(g)����H����H��ʾCH4��ȼ����
C�����º�ѹʱ����2 mol A��1 mol BͶ���ܱ������У�������Ӧ��2A(g)��B(g)?2C(g)����ַ�Ӧ���÷ų�������ΪQ kJ����÷�Ӧ�Ħ�H����Q kJ/mol
D����4P(s������)=P4(s������)����H����139.2 kJ/mol����֪���ױȰ����ȶ�
�ο��𰸣�D
���������A���з�Ӧ���������������������������ķ�Ӧ�����ȷ�Ӧ����Щ���ȷ�Ӧ���Է����У�B����CH4ȼ��δ�����ȶ���������CO2��C���з�Ӧ�ﲻ����ȫת�����ɺ���ת��Ϊ����Ϊ���ȷ�Ӧ�����Ե�����ʱ�����������ϸߣ���֪���ױȰ����ȶ���D����ȷ��
�㲦�����⿼�黯ѧ��Ӧ�����������ڿ��鿼����ȼ���ȡ��Ȼ�ѧ����ʽ�ȵ��������ж�������
�����Ѷȣ�һ��
2��ѡ���� ��б������������������ͬ�������壮��֪����S��s����б��+O2��g���TSO2?��g����H1=-297.16kJ?mol-1
��S��s��������+O2��g���TSO2?��g����H2=-296.83kJ?mol?-1?����˵����ȷ���ǣ�������
A��S��s������TS��s����������H3=+0.33kJ?mol?-1
B��������ȵ�б���ȶ�
C����ͬ���ʵ�����������ȵ�б�������е�������
D����ʽ��ʾ����lmol O2�й��ۼ������յ��������γ�1mol?SO2�й��ۼ����ų���������297.16KJ
�ο��𰸣���֪����S��s����б��+O2��g��=SO2 ��g����H1=-297.16kJ?mol-1 ����S��s��������+O2��g��=SO2 ��g����H2=-296.83kJ?mol -1��
��-�ڵõ��Ȼ�ѧ����ʽ��S��s����б��=S��s����������H3=-0.33kJ?mol -1��
A�����ݸ�˹���ɵõ��Ȼ�ѧ����ʽΪ��S��s����б��=S��s����������H3=-0.33kJ?mol -1����A����
B�������Ȼ�ѧ����ʽ��֪���������������ڵ�б�������������ȶ�����B��ȷ��
C����ͬ���ʵ�����������ȵ�б�������е������ͣ���C����
D����ʽ��ʾ����lmolO2�й��ۼ��Ͷ���S��s����б�������յ����������γ�1mol SO2�й��ۼ����ų���������297.16KJ����D����
��ѡB��
���������
�����Ѷȣ���
3��ѡ���� �ƾ�ȼ�յĹ����У�������������ת���������ж�����ȷ����
A����ѧ�ܲ���ת��Ϊ����
B�����ܲ���ת��Ϊ��ѧ��
C�����ܲ���ת��Ϊ��ѧ��
D�����ܲ���ת��Ϊ��ѧ��
�ο��𰸣�A
����������ƾ�ȼ���ǻ�ѧ�仯����ѧ����Ҫת��Ϊ���ܣ�����ת��Ϊ���ܣ���ѡA��
�����������dz�ʶ��֪ʶ�Ŀ��飬�ѶȲ�����ȷ��ѧ�ܵ�ת���ص��Ǵ���Ĺؼ�������������ѧ������˼ά�����ͷ�ɢ˼ά������
�����Ѷȣ���
4������� �Ĵ��зḻ����Ȼ����Դ������Ȼ��Ϊԭ�Ϻϳ����ص���Ҫ��������ͼ��ʾ(ͼ��ijЩת�����輰������δ�г�)��
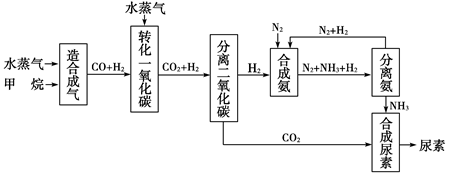
����д���пհף�
(1)��֪0.5 mol������0.5 molˮ������t �桢p kPaʱ����ȫ��Ӧ����һ��
��̼������(�ϳ���)��������a kJ�������÷�Ӧ���Ȼ�ѧ����ʽ�ǣ�______________________��
(2)�ںϳɰ���ʵ�����������У�����ȡ�Ĵ�ʩ֮һ�ǣ������ɵİ��ӻ�������м�ʱ����������������������ĵ���������ѭ�����ã�ͬʱ���䵪���������������û�ѧ��Ӧ���ʺͻ�ѧƽ��Ĺ۵�˵����ȡ�ô�ʩ�����ɣ�
________________________________________________________________��
(3)������ϳɰ�����ת����Ϊ75%ʱ����5.60��107 L����Ϊԭ���ܹ��ϳ�________L������(����������ڱ�״���²ⶨ)
(4)��֪���صĽṹ��ʽΪ ����д�����ֺ���̼��˫�������ص�ͬ���칹��Ľṹ��ʽ��
����д�����ֺ���̼��˫�������ص�ͬ���칹��Ľṹ��ʽ��
��__________________��?��_________________��
�ο��𰸣�(1)CH4(g)��H2O(g)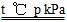 CO(g)��3H2(g) ��H����2a kJ��mol��1
CO(g)��3H2(g) ��H����2a kJ��mol��1
(2)��������������Ũ������������Ӧ���ʣ���С������Ũ�ȡ���������������Ũ�Ⱦ�������ƽ��������Ӧ�����ƶ�
(3)8.4��107
(4)�� ����NH4N��C��O
����NH4N��C��O
���������(1)0.5 mol CH4��ȫ��Ӧ����a kJ��������1 mol CH4��ȫ��Ӧ����2a kJ�������Ȼ�ѧ����ʽΪCH4(g)��H2O(g)=CO(g)��3H2(g)����H����2a kJ��mol��1��
(2)����ѭ����������������Ӧ��Ũ�ȣ�����Ӧ���ʣ����ת���ʣ�����NH3Ũ��������ƽ�������ƶ���
(3)�ɷ�Ӧ��ѧ����ʽ����ת����ϵ1CH4��3H2��2NH3��V(NH3)��5.60��107 L��75%��2��8.4��107 L��
(4)����д�� �ṹ����������������ӡ���д���칹��
�ṹ����������������ӡ���д���칹�� ��NH4N��C��O�Ľṹ��ʽ��
��NH4N��C��O�Ľṹ��ʽ��
�����Ѷȣ�һ��
5��ѡ���� ���з�Ӧ�У��������ȷ�Ӧ���ǣ�?��
A��ʵ������H2�ķ�Ӧ
B��ʵ������CO2�ķ�Ӧ
C����������������NH4Cl���巴Ӧ
D����ʯ����ˮ�ķ�Ӧ
�ο��𰸣�C
���������ʵ���Ҳ��ý������ᷴӦ�Ʊ��������÷�Ӧ���ڷ��ȷ�Ӧ����A����ѡ��ʵ������CO2�ķ�ӦΪ��ϡ������̼��Ʒ�Ӧ���÷�ӦҲ���ڷ��ȷ�Ӧ����B����ѡ����������������NH4Cl���巴Ӧ�������ȷ�Ӧ����CΪ����Ĵ𰸣���ʯ����ˮ�ķ�Ӧ���ڷ��ȷ�Ӧ����D��ѡ�����Ա���Ĵ�ѡ��C��
���������⿼���˻�ѧ��Ӧ�������ı仯������Ҫע��AB����ѡ���е���������Ϊʵ���ң����û��ע�����������������ѡ��������Ѷ��еȡ�
�����Ѷȣ���