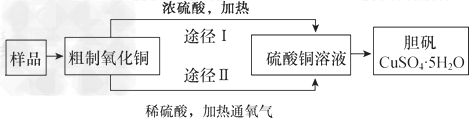
1、选择题 某课外研究小组,用含有较多杂质的铜粉样品,通过不同的化学反应制取胆矾。其实验过程如下:?下列叙述中不正确的是
[? ]
A.铜中含有大量的有机物,可采用灼烧的方法除去有机物
B.灼烧后含有少量铜的可能原因是该条件下铜无法被氧气氧化
C.通过途径Ⅱ实现用粗制氧化铜制取胆矾,必须进行的实验操作步骤:酸溶、加热通氧气、过滤、蒸发、冷却结晶、过滤、自然干燥
D.与途径Ⅱ相比,途径Ⅰ产生等量胆矾消耗硫酸少,且不会产生污染大气的气体
参考答案:D
本题解析:
本题难度:一般
2、实验题 酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、黏合剂及印刷、纺织等工业。乙酸乙酯的实验室和工业制法常采用如下反应CH3COOH+C2H5OH
CH3COOC2H5+H2O,请根据要求回答下列问题?
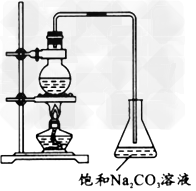
(1)欲提高乙酸的转化率,可采取的措施有______、____等。 ?
(2)若用图所示的装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为________、
________等。 ?
(3)此反应以浓硫酸为催化剂,可能会造成_________、_________等问题。
参考答案:(1)增大乙醇的浓度;移去生成物 ?
(2)原料来不及反应就被蒸出;温度过高,发生了副反应;冷凝效果不好,部分产物挥发了(任填两种) ?
(3)产生大量的酸性废液(或造成环境污染)?;部分原料炭化;催化剂重复使用困难;催化效果不理想(任填两种)
本题解析:
本题难度:一般
3、选择题 实验用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体经历下列过程,Fe3+在PH=5时已完全沉淀,其分析错误的是?

[? ]
A.用18mol/L浓硫酸配制溶解所用4mol/L的稀硫酸,玻璃仪器一般只有3种
B.利用Cu(OH)2替代CuO也可调试溶液pH不影响实验结果
C.洗涤晶体:向滤出晶体的漏斗中加少量水浸没晶体,自然流下,重复2-3次
D.若要用实验测定所得硫酸铜晶体中结晶水的数目要用到坩埚和坩埚钳
参考答案:A
本题解析:
本题难度:一般
4、实验题 淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图所示(加热、搅拌和仪器固定装置均已略去)
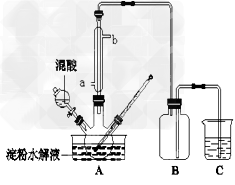
实验过程如下:
①将1∶1的淀粉水乳液与少许硫酸(98%)加入烧杯中,水浴加热至85℃~90℃,保持30?min,然后逐渐将温度降至60℃左右;
②将一定量的淀粉水解液加入三颈烧瓶中;
③控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液;
④反应3h左右,冷却,减压过滤后再重结晶得草酸晶体。硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3→6CO2+8NO↑+10H2O
3H2C2O4+2HNO3→6CO2+2NO↑+4H2O
请回答下列问题:
(1)实验①加入98%硫酸少许的目的是:_____________________。
(2)冷凝水的进口是________(填a或b);实验中若混酸滴加过快,将导致草酸产量下降,其原因是______________________。
(3)检验淀粉是否水解完全所用的试剂为____________________。
(4)草酸重结晶的减压过滤操作中,除烧杯、玻璃棒外,还必须使用属于硅酸盐材料的仪器有________________________。
(5)当尾气中n(NO2):n(NO)=1:1时,过量的NaOH溶液能将NOx全部吸收,发生的化学反应为:NO2+NO+2NaOH=2NaNO2+H2O,若用含硫酸的母液来吸收氮氧化物,其优点是
___________、缺点是____________。
(6)?将产品在恒温箱内约90℃以下烘干至恒重,得到二水合草酸。用KMnO4标准溶液滴定,该反应的离子方程式为:2MnO4-?+?5H2C2O4?+?6H+?=?2Mn2+?+?10CO2↑+?8H2O 称取该样品0.12?g,加适量水完全溶解,然后用0.020?mol・L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),此时溶液颜色由_______变为________。滴定前后滴定管中的液面读数如图所示,则该草酸晶体样品中二水合草酸的质量分数为__________________。

参考答案:(1) 加快淀粉水解的速度(或起到催化剂的作用)
(2) a;温度过高 、硝酸浓度过大,导致H2C2O4进一步被氧化?
(3) 碘水或KI-I2溶液?
(4) 布氏漏斗、吸滤瓶 (安全瓶、抽气泵不作为主要仪器)?
(5) 优点:提高HNO3利用率(或循环使用氮氧化物);缺点:NOx(或氮氧化物)吸收不完全
(6)无色;紫红色(或淡紫色);84.0%
本题解析:
本题难度:一般
5、实验题 聚合硫酸铁(PFS)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。现用一定质量的铁的氧化物(如下图)为原料来制取聚合硫酸铁,为控制水解时Fe3+的浓度,防止生成氢氧化铁沉淀,原料中的Fe3+必须先还原为Fe2+。实验步骤如下:
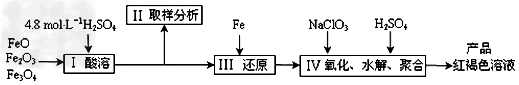
(1)实验室用18.4?mol・L-1的浓硫酸量取_______mL来配制250mL4.8?mol・L-1的硫酸溶液,所用的仪器除烧杯、玻璃棒和移液管外,还需要的玻璃仪器_____________。
(2)步骤II取样分析溶液中的Fe2+、Fe3+的含量,目的是_____________。
A.控制溶液中Fe2+与Fe3+含量比?
B.确定下一步还原所需铁的量
C.确定氧化Fe2+所需NaClO3的量?
D.确保铁的氧化物酸溶完全
(3)①写出步骤Ⅳ中用NaClO3氧化时的离子方程式____________________(提示:ClO3-转化为Cl-);
②已知1mol?HNO3的价格为0.16元,1mol?NaClO3的价格为0.45元,评价用HNO3代替NaClO3作为氧化剂的利弊,利是__________,弊是____________。
(4)为了分析产品聚合硫酸铁溶液中SO42-与Fe3+?物质的量之比,有人设计了以下操作
(a)取25mL聚合硫酸铁溶液,加入足量的BaCl2溶液,产生白色沉淀,白色沉淀经过过滤、洗涤、干燥后,称重,其质量为m?g。
(b)另取25mL聚合硫酸铁溶液,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗液合并配成250mL溶液,取该溶液25.00mL,用KMnO4酸性溶液滴定,到达终点时用去0.1000?mol/L?KMnO4标准溶液VmL。离子方程式为:5Fe2+?+?MnO4-+?8H+?=?5Fe3+?+?Mn2+?+?4H2O
①判断(a)步骤溶液中SO42-离子已沉淀完全的方法是__________________;?
②在(b)步骤中判断达到终点的现象是_______________;
③聚合硫酸铁中SO42-与Fe3+的物质的量之比为____________(用含m、V的代数式表示)。
参考答案:(1)65.2mL;250mL容量瓶、胶头滴管
(2)BC
(3)①6Fe2+ + ClO3- + 6H+ = 6Fe3+ + Cl- + 3H2O
②利:原料成本较低;弊:产生气体对大气有污染
(4)①取上层清夜,滴加BaCl2溶液,若无沉淀产生,则溶液中SO42-已沉淀完全;②溶液由浅蓝色变为浅紫红色,且半分钟内不变色;③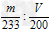
本题解析:
本题难度:一般