1、简答题 为了制得较纯净的Fe(OH)2,甲乙两同学分别用下面两种方法制得白色的Fe(OH)2沉淀.
同学甲:用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备.
(1)用硫酸亚铁晶体配制上述FeSO4溶液时还需加入______.
(2)除去蒸馏水中溶解的O2常采用______的方法.
(3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液.
同学乙:在如图装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备.A管中是Fe和H2SO4,B管中是NaOH溶液.
(4)先打开a,使A管中反应一段时间后再夹紧止水夹a,这样做的目的是______.
(5)A管中发生反应的离子方程式为______
(6)B管中生成沉淀的离子方程式为______.
(7)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是______.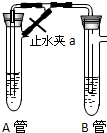
参考答案:(1)硫酸亚铁易被氧化而变质,可加入铁粉,故答案为:Fe粉;
(2)除去蒸馏水中溶解的O2常采用加热的方法,原因是加热时气体的溶解度降低,故答案为:加热;
(4)A管中产生的气体通入B管中排尽B管中的空气,使B充满还原性气体氢气,可排除试管中的氧气,可防止生成的
Fe?(OH)2被氧化,
故答案为:A管中产生的气体通入B管中排尽B管中的空气,使B充满还原性气体氢气;
(5)Fe和酸反应生成氢气和亚铁离子,反应的离子方程式为Fe+2H+=Fe2++H2↑,故答案为:Fe+2H+=Fe2++H2↑;?
(6)B管中生成沉淀为Fe(OH)2,反应的离子方程式为Fe2++2OH-=Fe(OH)2↓,故答案为:Fe2++2OH-=Fe(OH)2↓;
(7)Fe(OH)2易被氧化而变质,试管A中反应生成的H2充满了A试管和B试管,且外界空气不容易进入,
故答案为:试管A中反应生成的H2充满了A试管和B试管,且外界空气不容易进入.
本题解析:
本题难度:一般
2、选择题 下列实验装置图操作正确的是( )
A.
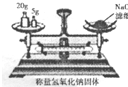
称量氢氧化钠固体
B.
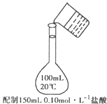
配置150mL?0.10mol?L-1盐酸
C.
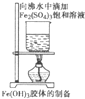
Fe(OH)3液体的制备
D.
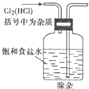
除杂
参考答案:C
本题解析:
本题难度:简单
3、选择题 下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是
[? ]
①向饱和碳酸钠溶液中通入过量的CO2
②向Fe(OH)3胶体中逐滴加入过量的稀硫酸
③向AgNO3溶液中逐滴加入过量氨水
④向硅酸钠溶液中逐滴加入过量的盐酸
A.①②
B.①③
C.①④
D.②③
参考答案:C
本题解析:
本题难度:一般
4、选择题 下列实验原理及装置合理的是( )
A.
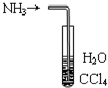
吸收NH3防止倒吸
B.
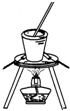
从食盐水中提取NaCl
C.
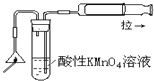
检验火柴头燃烧产生的SO2
D.
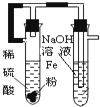
制备Fe(OH)2
参考答案:A
本题解析:
本题难度:简单
5、选择题 以下物质间的转化中,其中有不能通过一步反应实现的是
[? ]
A.Fe - FeCl2 - Fe(OH)2 - Fe(OH)3
B.Al - Al2O3 - Al(OH)3 - NaAlO2
C.S - SO2 -H2SO4 - MgSO4
D.N2 - NO - NO2 - HNO3
参考答案:B
本题解析:
本题难度:简单