1、填空题 附加题(1)石墨晶体的层状结 构,层内为平面正六边形结构(如图a),试回答下列问题:图中平均每个正六边形占有C原子数为____个、占有的碳碳键数为____个,碳原子数目与碳碳化学键数目之比为_______。
构,层内为平面正六边形结构(如图a),试回答下列问题:图中平均每个正六边形占有C原子数为____个、占有的碳碳键数为____个,碳原子数目与碳碳化学键数目之比为_______。
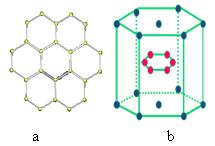
(2)2001年报道的硼和镁形成的化合物刷新了金属化合物超导温度的最高记录。如图 b所示的是该化合物的晶体结构单元:镁原子间形成正六棱柱,且棱柱的上下底面还各有1个镁原子,6个硼原子位于棱柱内。则该化合物的化学式可表示为______
b所示的是该化合物的晶体结构单元:镁原子间形成正六棱柱,且棱柱的上下底面还各有1个镁原子,6个硼原子位于棱柱内。则该化合物的化学式可表示为______ _。
_。
参考答案:(1)2? 3? 2:3?(2)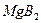
本题解析:略
本题难度:简单
2、选择题 下列不是离子化合物的是
A.H2O
B.CaI2
C.KOH
D.NaNO3
参考答案:A
本题解析:略
本题难度:一般
3、选择题 朱经武(Paul Chu)教授等发现钇钡铜氧化合物在90K时即具有超导性,该化合物的部分结构如图产所示:
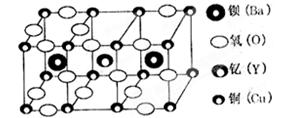
该化合物以Y2O3、BaCO3和CuO为原料,经研磨烧结而成,其原料配比(物质的量之比)为
A.1:1:1
B.1:4:6
C.1:2:3
D.2:2:3
参考答案:B
本题解析:略
本题难度:一般
4、填空题 【化学―选修3 物质结构与性质】(15分)
A、B、C、D、E是原子序数逐渐增大的1-36号元素。A原子核外有4个原子轨道填充了电子;B的第一电离能比同周期相邻元素的第一电离能大,其气态氢化物在水中的溶解度在同族元素氢化物中最大;C的最高化合价和最低化合价的代数和为4;D原子的M层和N层电子数均比E原子少4个,E是人体必须的微量元素。
试根据 以上信息,回答下列问题:
以上信息,回答下列问题:
(1)A原子的电子排布图?,E原子的外围电子排布式为?。
(2)AC2分子中含有?个π键。
(3)含C50%的C的氧化物的空间构型为_________,C的原子轨道采用______杂化。
(4)写出A的常见氧化物与B的氧化物中互为等电子体的一组?。
(5)已知D的晶体在不同温度下有A、B两种堆积方式,则A、B两晶胞中D原子的配位数之比?; 晶体的密度之比为?。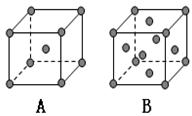
参考答案:
(1)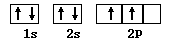 (1分)? 4S24P4 (2分)
(1分)? 4S24P4 (2分)
(2)2?(2分)?(3)V形?(2分)? SP2 (2分)
(4)CO2、N2O (2分)?(5)2 :3 (2分)?约0.92(2分)
本题解析:略
本题难度:一般
5、填空题 (22分) 乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
(1) CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为??;1mol O22+中含有的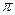 键数目为?。
键数目为?。
(2)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2,红棕色沉淀。Cu+基态核外电子排布式为?。
(3)乙炔与氢氰酸反应可得丙烯腈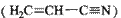 。丙烯腈分子中碳原子轨道杂化类型是??;分子中处于同一直线上的原子数目最多为?。
。丙烯腈分子中碳原子轨道杂化类型是??;分子中处于同一直线上的原子数目最多为?。
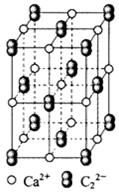
(4) CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),但CaC2晶体中哑铃形C22-的存在,使晶胞沿一个方向拉长。CaC2晶体中1个Ca2+周围距离最近的C22-数目为??。
(5)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇的沸点比甲醛高,其主要原因是?;甲醛分子中碳原子的轨道杂化类型为?。
②甲醛分子的空间构型是?;1mol甲醛分子中σ键的数目为?。
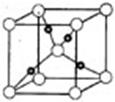
③在1个Cu2O晶胞中(结构如图所示),所包含的Cu原子数目为?。
参考答案:

③4
本题解析:略
本题难度:简单