1、简答题 原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族.
(1)W元素在周期表中的位置为______;写出Y元素原子的价电子排布式:______;
(2)由X、Z两元素可以组成A、B两种化合物,A在一定条件下可以分解成B,A的分子属于______(填“极性”、“非极性”)分子.
(3)一定条件下,Y的单质气体与X的单质气体充分反应生成6.8g?C气体(已知n(X):n(Y)=3:1)可放出18.44kJ热量,则该反应的热化学方程式为______.
(4)由X、Y、Z、W四种元素组成的一种离子化合物D
①已知1mol?D能与足量NaOH浓溶液反应生成标准状况下44.8L气体.写出加热条件下D与NaOH溶液反应的离子方程式______.
②又知D既能与盐酸反应,又能与氯水反应,写出D与氯水反应的离子方程式______.
(5?)X的单质与Z的单质在KOH的浓溶液中可以形成原电池,如果以金属M和金属N为惰性电极,在电池的M极通入X的单质气体,N极通入Z的单质气体,则M极的电极反应式为______.
2、选择题 下列有关“核外电子的运动状态”的说法,错误的是( )
A.各原子轨道的伸展方向按p、d、f的顺序分别为3、5、7
B.核外电子云表示电子在核外单位体积的空间出现的机会多少
C.原子轨道伸展方向与能量大小是无关的
D.原子核外可能有两个电子的运动状态是完全相同的
3、填空题 下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素
试回答下列问题:
(1)表中第一电离能最小的是______(填字母,下同),第一电离能最大的是______.c、d、e三种元素的第一电离能由大到小的顺序是______,它们与a元素形成的最简单化合物的热稳定性由强到弱的是______(填化学式).
(2)第三周期中由电负性最大的元素与电负性最小的元素组成的化合物化学式是______.
(3)表中基态原子的未成对电子数最多的元素是______,其二价阳离子的外围电子排布式是______.
(4)写出由a、d、e三种元素组成的一种离子化合物的化学式______,并用离子方程式来说明其水溶液显酸性的原因______.
4、选择题 在基态多电子原子中,关于核外电子能量的叙述错误的是
[? ]
A.最易失去的电子能量最高
B.电离能最小的电子能量最高
C.p轨道电子能量一定高于s轨道电子能量
D.在离核最近区域内运动的电子能量最低
5、简答题 化学选做题----物质结构
铜是过渡元素.化合物中,铜常呈现+1价或+2价.
(1)写出Cu+的电子排布式______.
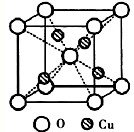
(2)如图为某铜矿晶体结构单元,该铜矿的化学式______.
(3)已知,铜的第一电离能为746kJ?mol-1,第二电离能为1958kJ?mol-1.请结合核外电子排布相关知识解释,铜第二电离能远远大于第一电离能的原因______
(4)对于CuX(X为卤素)而言,铜与X形成的化学键极性越强,对应的CuX的溶解度越大.据此可知,CuCl的溶解度比CuI的溶解度______(填“大”或“小”).
(5)CO、NH3都能提供孤电子对与Cu+形成配合物.Cu+与NH3形成的配合物可表示为[Cu(NH3)?n]+.该配合物中,Cu+的4s轨道及4p轨道通过sp杂化接受NH3提供的孤电子对.
①[Cu(NH3)n]+中n=______;
②[Cu(NH3)n]+中Cu+与n个氮原子构成的空间结构呈______型.
③[Cu(NH3)?n]+溶液可用于吸收合成氨原料气中的CO,加热吸收CO后的溶液又将放出CO.加热分解放出CO的过程中,必须克服微粒间的作用力是______.