1��ʵ���� ��ѧ�̲ĸ��л�ѧ��һ��������ͼ1��ʾ��ͭ��Ũ���ᷴӦʵ��װ�ã���ʵ������л��ж�����������ų�����Ⱦ���ڿ��������ص���ʦ��������Ϊ��ij����С��Դ�ʵ�������ͼ2��ʾ�ĸĽ����Ľ���ʵ��������������ԣ����Ҽ���������������й©��ʵ�鲽�����£�
 ?
?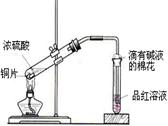
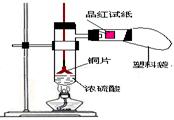
 ͼ1?ͼ2
ͼ1?ͼ2
 �����Ȱ�װ��ͼ��װ��������װ����ʱ����֧�ܽ�������˿���Ϲ�һƬƷ����ֽ��
�����Ȱ�װ��ͼ��װ��������װ����ʱ����֧�ܽ�������˿���Ϲ�һƬƷ����ֽ��
 ���������Թ��м���Լ10������Ũ���ᣬ���ȣ��ڼ���Ũ����ʱ����ͭƬ��������ͭƬ�Ȳ�Ҫ����Ũ�����У���������������ʱ����ͭƬ���£�ʹ����ȫ����Ũ�����У���Ӧ���̷������Ȳ���Ҫ��Ӧʱֹͣ���Ȳ���ͭƬ�����뿪Ũ���ᣬ��Ӧ��ֹͣ�ˡ�
���������Թ��м���Լ10������Ũ���ᣬ���ȣ��ڼ���Ũ����ʱ����ͭƬ��������ͭƬ�Ȳ�Ҫ����Ũ�����У���������������ʱ����ͭƬ���£�ʹ����ȫ����Ũ�����У���Ӧ���̷������Ȳ���Ҫ��Ӧʱֹͣ���Ȳ���ͭƬ�����뿪Ũ���ᣬ��Ӧ��ֹͣ�ˡ�
 �ش��������⣺
�ش��������⣺
 ��1����ͼ2��ʾ��ͭƬ����ڵ�Ũ����Ӵ���ɿ����������У���?��
��1����ͼ2��ʾ��ͭƬ����ڵ�Ũ����Ӵ���ɿ����������У���?��
 ��2�����ϴ������ǣ�����������������������������������
��2�����ϴ������ǣ�����������������������������������
 ��3��Ϊ�˷�ֹ��Ӧ�����������Թ��е���������ϴ��е�������Ⱦ�������ɽ��еIJ����ǣ�?����ص����ӷ���ʽ�ǣ�?��
��3��Ϊ�˷�ֹ��Ӧ�����������Թ��е���������ϴ��е�������Ⱦ�������ɽ��еIJ����ǣ�?����ص����ӷ���ʽ�ǣ�?��
�ο��𰸣���1��֧�ܿ��а������Թ��г�����ɫ��Ʒ����ֽ��ɫ��ͭƬ�����ܽ⡣
 ?��2���ռ������SO2���壬��ֹ��Ⱦ������
?��2���ռ������SO2���壬��ֹ��Ⱦ������
 ��3���ڷ�Ӧ����Թ��С����ϴ��м������ļ�����SO2����?
��3���ڷ�Ӧ����Թ��С����ϴ��м������ļ�����SO2����?
 SO2+2OH-
SO2+2OH-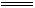 H2O+SO32-��SO2+OH-
H2O+SO32-��SO2+OH-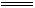 HSO3-
HSO3-

�����������ͭƬ�Ӵ���Ũ����ʱ���д����İ������������������ڶ�������������ˮ����γ�������СҺ��Ե�ʣ�����֧�ܿ�����Ʒ����ֽ�ϣ�ʹƷ����ֽ�ĺ�ɫ��ʼ��ɫ������ԭ����ɫ������Һ��ʼ���̣���Ʒ����ֽ��ȫ�ʳɰ�ɫ��ͭƬ������ʹ���뿪Ũ������Һ����Ӧ����ֹͣ��
�����Ѷȣ�һ��
2��ʵ���� ��9�֣�ijС��ͬѧΪ̽��ͭ��Ũ����ķ�Ӧ��������ռ�һƿ��Ӧ���������壬���������ͼ��ʾװ�á�ʵ��������ȡ6.4gͭƬ��12mL 18mol/LŨ�������Բ����ƿ�м��ȣ�ֱ����Ӧ����Է�����ƿ����ͭʣ�ࡣ

��1��Ϊ��ֹ������Ⱦ���벹����ͼ����е�ʵ��װ�ã���ע������Ҫ���Լ����ơ�
��2��д��ͭ��Ũ���ᷴӦ�Ļ�ѧ����ʽ��
?��
��3����С����ΪͭƬδ��ȫ�ܽ⣬��ƿ�п��ܻ���һ����������ʣ�࣬��ԭ���ǣ�
?��
��4��Ϊ֤����Ӧ���������ƿ��ȷ�����ᣬ��ѡ������ҩƷ�е�?����д��ĸ��ţ���
A������
B��BaCl2��Һ
C������
D��Na2CO3��Һ
�ο��𰸣�

�����������1��Ϊ��ֹ������Ⱦ��Ӧ��β������װ�ã�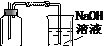
��2��д��ͭ��Ũ���ᷴӦ�Ļ�ѧ����ʽ��Cu��2H2SO4(Ũ)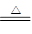 CuSO4��SO2��+2H2O
CuSO4��SO2��+2H2O
��3����С����ΪͭƬδ��ȫ�ܽ⣬��ƿ�п��ܻ���һ����������ʣ�࣬��ԭ���ǣ�
ֻͭ��Ũ���ᷴӦ�����ŷ�Ӧ�Ľ��У�Ũ�����Ϊϡ���ᣬͭ�Ͳ��ڷ�Ӧ�����ԣ���Һ�п϶���ϡ������ڡ�
��4��Ϊ֤����Ӧ���������ƿ��ȷ�����ᣬ��ѡ�õ�ҩƷ�����ۡ�Na2CO3��Һ���������ۣ���������ܽⲢ�����ݲ�����֤�������ᡣ����Na2CO3��Һ����������ݲ�����֤�������ᡣ��ѡA D��
�����Ѷȣ���
3������� ���������ʵ�飬���������ַ���֤����������Աȴ��������ǿ��
�ɹ�ѡ��ѡ����Լ���0.1mol/L��HCl��0.1mol/L��CH3COOH��0.1mol/L��NaOH��0.1mol/L��CH3COONa��CaCO3��ĩ��PH��ֽ������ˮ����̪��Һ��ʯ����Һ��������������ѡ��
�ο��𰸣�֤����������Աȴ��������ǿ�ķ����У��ⶨ��ͬŨ�ȴ����������Һ��PHֵ��С������ͬŨ�ȵ�����ʹ���ֱ��̼��Ʒ�Ӧ�����ݷ�Ӧ�����жϣ�ͨ���Ƚ������ͬ��pH��ͬ������Һͬ����ϡ�ͺ���Һ��pH�仯��С������ȣ�
ʵʩ�����У�
�ٷֱ�ȡ����pH��ֽ���ڲ���Ƭ�ϣ��ò������ֱ�պȡ0.1mol/L��HCl��0.1mol/L��CH3COOH��pH���ñ���ɫ�����գ�pHС��Ϊǿ�ᣬ���Ϊ���ᣮ
��ȡ����̼��Ʒ�ĩ����ֻ�Թ��У��ٷֱ����������0.1mol/L��HCl��0.1mol/L��CH3COOH����Ӧ�Ͼ��ҵ�Ϊǿ�ᣬ��Ӧ�����ҵ�Ϊ���ᣮ
��֤����������Աȴ��������ǿ�ķ���Ϊ�ٷֱ�ȡ����pH��ֽ���ڲ���Ƭ�ϣ��ò������ֱ�պȡ0.1mol/L��HCl��0.1mol/L��CH3COOH��pH���ñ���ɫ�����գ�pHС��Ϊǿ�ᣬ���Ϊ�����ȡ����̼��Ʒ�ĩ����ֻ�Թ��У��ٷֱ����������0.1mol/L��HCl��0.1mol/L��CH3COOH����Ӧ�Ͼ��ҵ�Ϊǿ�ᣬ��Ӧ�����ҵ�Ϊ���ᣮ
���������
�����Ѷȣ�һ��
4��ʵ���� ��7�֣�ij�о�С��Ϊ��̽�������������Ӧ���������˼���ʵ�顣����д���пհף�
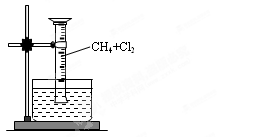
��ʵ��һ������ͼ��ʾװ�ã���ˮ���ռ�һ�Թܼ���������Ļ�����壬���պ�۲쵽��Ͳ���γ�һ��ˮ������Ϊ���Ȼ������ɡ�
��1���÷�Ӧ�Ļ�ѧ����ʽΪ?��ֻд��һ�������÷�Ӧ����?���Ӧ���ͣ�
��2��ˮ����ʢ�ŵ�Һ�����Ϊ?�������ţ�
A��ˮ
B������ʯ��ˮ
C������ʳ��ˮ
D������NaHCO3��Һ