1、实验题 (7分)某化学兴趣小组为了探究在常温下某非金属氧化物形成的未知气体的成分。该小组成员将气体通入澄清石灰水,发现变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想。
猜想1:?;
猜想2:?;
猜想3:?。
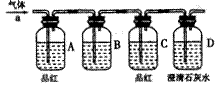
为了验证猜测,该小组设计实验加以探究:该小组同学按如图所示装置,将气体从a端通入,则:(1)B中应该装下列?试剂(填编号)
A.氢氧化钠溶液? B酸性高锰酸钾溶液
C.饱和碳酸钠溶液? D.饱和碳酸氢钠溶液
(2)A中品红的作用是:?
(3)D中澄清石灰水的作用是:?
通过该实验,该小组同学观察到以下三个实验现象:①A中品红褪色②C中品红不褪色③ D中澄清石灰水变浑浊。由此得出结论:该气体的成分为?。
参考答案:(7分)(每空1分)
该气体是SO2气体;该气体是CO2气体;?该气体是SO2,CO2的混合气体
(1)B? (2)检验SO2的存在(3)检验CO2的存 在;该气体是SO2,CO2的混合气体
在;该气体是SO2,CO2的混合气体
本题解析:略
本题难度:一般
2、选择题 清蒸大闸蟹由青色变成红色,一同学认为这种红色物质可能象酸碱指示剂一样,遇到酸或碱颜色会发生改变。就这位同学的看法而言,这应该属于科学探究中的
[? ]
A.实验
B.假设
C.观察
D.分类
参考答案:B
本题解析:
本题难度:简单
3、填空题 欲用浓硝酸法(测定反应后生成气体的量)测定某铜银合金中铜的质量分数,但资料表明:
①反应中除生成NO2气体外还会有少量的NO生成;
②常温下NO2和N2O4混合存在,在低于0℃时几乎只有无色的N2O4液体或晶体存在。
为完成测定并验证有NO生成,有人没计如F实验装置:
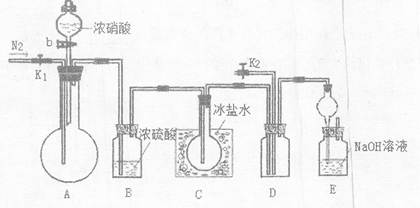
(1)实验开始前要先打开A部分的活塞K1,持续通一段时间的氮气再关闭K1,这样做的目的是?。
(2)装置中B瓶的作用是?。
(3)实验时A中反应停止后,打开D装置导管的活塞K2并通入氧气,若反应确有NO产生,D中的现象是?;实验时发现通入氧气温度的高低对实验有较大的影响,为便于观察应通入____(填“冷”或“热”)的氧气,其原因是:____
(4)若实验只测定Cu的质量分数,不检验NO的产生,则在铜银合金与浓硝酸反应后,只需加入过量的____(填一种物质的化学式,下同)溶液,过滤、洗涤、干燥称量?的质量就可达目的。(已知Cu(OH)2与AgOH类似,也可以溶于过量的氨水而形成溶液。)
参考答案:
本题解析:略
本题难度:一般
4、选择题 下列关于研究物质性质的基本程序,排列顺序正确是
[? ]
a、观察物质的外观b、实验和观察c、解释及结论d、预测物质的性质
A.b a c d
B.a d b c
C.a b c d
D.d a b c
参考答案:B
本题解析:
本题难度:简单
5、实验题 在进行某实验探究过程中,一些学生发现等质量的铜片分别与等体积(均过量)的浓硝酸和稀硝酸反应,所得溶液前者为绿色,后者为蓝色。
针对这种现象,学生们进行了讨论后,出现了以下两种观点:
一种认为,这可能是Cu2+浓度的差异引起的。你同意这种看法吗??(填“同意”或“不同意”),原因是?。
另一种认为,呈“绿色”是Cu2+与NO2混合的结果。请你设计出一个实验方案证明之,你设计的实验方案是??
已知0.3mol Cu与足量的稀硝酸反应,则被还原的HNO3的物质的量是?mol。
参考答案:不同意(1分)?浓硝酸、稀硝酸均过量,Cu全部转化为Cu2+,则在同体积的溶液中Cu2+浓度相同、溶液颜色应该相同(2分)
加水稀释看能否由绿色变为蓝色(2分,其它合理答案均可)
0.2mol(2分)
本题解析:因溶液的颜色由有色离子的浓度来决定,而Cu2+浓度相同,颜色应该相同,故答案为:不同意; 浓硝酸、稀硝酸均过量,Cu全部转化为Cu2+,则在同体积的溶液中Cu2+浓度相同、溶液颜色应该相同。
因除去NO2若颜色变蓝,则是由于Cu2+与NO2混合的结果,故答案为:加水稀释看能否由绿色变为蓝色。
Cu与足量的稀硝酸反应:3Cu+8HNO3===3Cu(NO3)2+2NO↑+4H2O,在这个方程式中我们可以知道有2mol硝酸被还原成NO,参加反应的硝酸与被还原的硝酸的物质的量之比是4:1,而0.3molCu和0.8molHNO3完全反应,所以硝酸物质的量为0.8mol,则被还原的HNO3物质的量是0.2mol。
点评:本题主要考查了铜与硝酸的反应,根据问题情景,运用所学知识来解决问题,培养了学生分析问题解决问题的能力,题目难度中等。
本题难度:一般