1、填空题 (8分)、钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”。试回答下列问题:
(1)钛有 Ti和
Ti和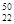 Ti两种原子,它们互称为?。Ti元素在元素周期表中的位置是第??周期,第??族;按电子排布Ti元素在元素周期表分区中属于?(填s、p、d、ds或f)区元素
Ti两种原子,它们互称为?。Ti元素在元素周期表中的位置是第??周期,第??族;按电子排布Ti元素在元素周期表分区中属于?(填s、p、d、ds或f)区元素
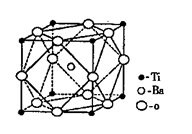
(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用。偏钛酸钡为离子晶体,晶胞的结构如右图所示,它的化学式是?
(3)现有含Ti3+的配合物,化学式为TiCl3(H2O)6,将1mol该物质溶于水,加入足量硝酸银溶液,立即沉淀的氯化银为1mol,已知该配合物的配位数为6,则该配合物的配位体是?。
1mol该配合物外界所含结晶水物质的量为?mol。
2、填空题 (9分)

 某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表:(1)请从下表中实验现象(Ⅱ)(填A、B、C……)中选出与方案(I)(填1、2、3……)对应的实验现象,填入答案(Ⅲ)中。
某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表:(1)请从下表中实验现象(Ⅱ)(填A、B、C……)中选出与方案(I)(填1、2、3……)对应的实验现象,填入答案(Ⅲ)中。

实验方案(I)
| 实验现象(Ⅱ)

| 答案(III)
|
实验方案I
| 实验现象II
|
1.用砂纸擦后的镁带与沸
 水反应,再向反应液中滴 水反应,再向反应液中滴
 加酚酞 加酚酞
| A浮与水面,剧烈反应,放出气体,
 熔成―个小球,在水面上无定向移 熔成―个小球,在水面上无定向移
 动,随之消失,溶液变红色。 动,随之消失,溶液变红色。
| 1
| ?
|
2.向新制的H2S饱和溶
 液中滴加新制的氯水 液中滴加新制的氯水

| B.产生大量气体,可在空气中燃
 烧,溶液变成浅红色 烧,溶液变成浅红色

| 2
| ?
|
3.钠与滴有酚酞的冷水反应

| C.反应不十分剧烈,产生的气体
 可以在空气中燃烧 可以在空气中燃烧

| 3
| ?
|
4.镁带与2mol/L的盐酸
 反应 反应

| D.剧烈反应,产生的气体可以在
 空气中燃烧 空气中燃烧

| 4
| ?
|
5铝条与2mol/L的盐酸
 反应 反应
| E.生成白色絮状沉淀,继而沉淀
 消失 消失

| 5
| ?
|
6.向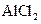 溶液中滴加 溶液中滴加
 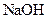 溶液至过量 溶液至过量

| F.生成淡黄色沉淀

| 6
| ?
|
(2)通过以上实验分析了同周期元素的符号?,从实验结果可以得出的结论是?。
3、选择题 应用元素周期律的有关知识,可以预测我们不知道的一些元素及其化合物的性质。下列预测中不正确的是(?)
①Be的最高价氧化物的水化物可能具有两性?
②H2Se是无色,有毒,比H2S稳定的气体
③At单质为有色固体,AgAt不溶于水也不溶于稀硝酸?
④Li在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱?
⑤SrSO4是难溶于水的白色固体?
⑥B和Si的最高价氧化物的水化物均为H2XO3形式,且酸性很弱
A.①②③④
B.②④⑥
C.①③⑤
D.②④⑤
4、选择题 能说明Cl的非金属性比S的非金属性强的事实是
A.Cl2与H2反应生成HCl,而S与H2反应生成H2S
B.Cl2与铁反应生成FeCl3,而S与铁反应生成FeS
C.Cl2能与水反应,而S不与水反应
D.Cl原子最外层电子数为7,而S原子最外层电子数为6
5、选择题 某课外兴趣小组通过实验发现钾和钠的性质相似,下列说法中能最好地解释这个事实的是(? )
A.都是金属元素
B.原子半径相差不大
C.最外层电子数相同
D.最高化合价相同