1、选择题 一种新型燃料电池,以镍板为电极插入KOH溶液中,分别向两极通入乙烷和氧气。电极反应式为:C2H6 +180H- -14e-="=" 2C032一+ 12H20;? 7H20+7/2 02+14e - ="=140H" -.
下列有关此电池的推断错误的是?(?)
A.在电解质溶液中OH -向正极移动
B.参加反应的02与C2H6的物质的量之比为7:2
C.放电一段时间后,KOH的物质的量浓度将下降
D.通氧气的电极为正极
参考答案:A
本题解析:略
本题难度:一般
2、填空题 铁及铁的化合物应用广泛,如FeCl3可用作印刷电路铜版腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路板的离子方程式____________________。
(2)若将(1)中的反应设计成原电池,请在方框内画出原电池的装置图,标出正、负极,并写出电极反应式。 负极反应:____________________; 正极反应:____________________。

参考答案:(1)2Fe3++Cu==Cu2++2Fe2+
(2)Cu-2e-==Cu2+;2Fe3++2e-==2Fe2+;原电池图:“略”
本题解析:
本题难度:一般
3、选择题 研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电。关于该电池的下列说法不正确的是
A.水既是氧化剂又是溶剂
B.放电时正极上有氢气生成
C.放电时OH-向正极移动
D.总反应为:2Li+2H2O="==" 2LiOH+H2↑
参考答案:C
本题解析:考生可能迅速选出C项是错误,因为原电池放电时OH-是向负极移动的。这个考点在备考时训练多次。这种电池名称叫锂水电池。可推测其总反应为:2Li+2H2O="==" ?2LiOH+H2↑。再写出其电极反应如下:(―)2Li―2e―=2Li+?(+)2H2O+2e―=2OH―+H2↑
结合选项分析A、B、D都是正确的。此题情景是取材于新的化学电源,知识落脚点是基础,对原电池原理掌握的学生来说是比较容易的。
本题难度:一般
4、简答题 有铜片、锌片和250mL稀硫酸组成的原电池,当在铜片上放出4.48L(标准状况下)的气体时,硫酸恰好完全反应.
(1)该原电池的正极反应式______
(2)原稀硫酸的物质的量浓度是______mol/L
(3)锌片减少的质量______.
参考答案:(1)锌的活泼性大于铜,所以锌片作负极,铜片作正极,正极上氢离子得电子生成氢气.
故答案为:2H++2e-=H2 ↑.
(2)Zn+H2SO4 =ZnSO4 +H2↑
? 1mol? 22.4L
?0.2 mol?4.48L
硫酸的物质的量为? 0.2 mol,所以其物质的量浓度为C=nV=0.2?mol0.25L=0.8mol/L
故答案为0.8;
?(3)Zn+H2SO4 =ZnSO4 +H2↑
?65g? 22.4L
?13g?4.48L
故答案为:13g;
本题解析:
本题难度:一般
5、选择题 将下图中所示实验装置的K闭合,下列判断正确的是
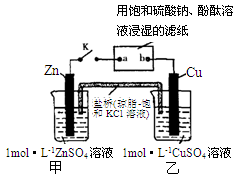
A.电子沿Zn→a→b→Cu路径流动
B.Cu电极上发生氧化反应
C.甲池与乙池中的溶液互换,闭合K仍有电流产生
D.片刻后可观察到滤纸a点变红色