1、填空题 (1)上表中的实线是元素周期表部分边界,请在表中用实线画出金属元素的边界(实线内的元素全是金属元素)
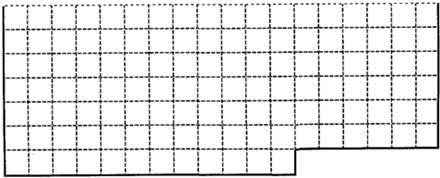
(2)元素甲是第三周期ⅦA族元素,化合物A是由甲元素等非金属元素组成的离子化合物写出其化学式______,
(3)元素乙是第三周期原子半径最小的金属元素,丙是短周期元素中原子半径最大的元素,用电子式表示丙在空气中加热反应生成B的形成过程______.B中含有的化学键是______
(4)化合物C是由甲元素和乙元素形成的化合物,将化合物A与化合物C等物质的量溶于水中,向其中滴加过量的2mol?L-1氢氧化钠溶液,直至形成透明溶液.请根据实验现象出现的先后顺序,依次写出离子方程式:__________________.
(5)实验中丙元素的鉴别方法______(不写过程)与现象______.
参考答案:(1)元素周期表的结构以及元素的分布情况,表示元素周期表的部分边界如下:
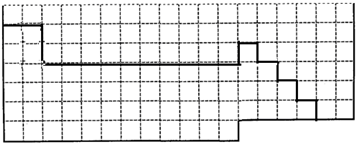
,故答案为:

;
(2)第三周期ⅦA族元素是Cl,由Cl元素等非金属元素组成的离子化合物是氯化铵,故答案为:NH4Cl;
(3)第三周期原子半径最小的金属元素为Al,短周期元素中原子半径最大的元素是Na,钠在空气中加热反应生成过氧化钠,它的形成过程可以表示为:
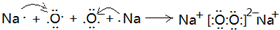
,在过氧化钠中,钠离子和过氧根之间是离子键,过氧根中氧和氧之间是共价键,故答案为:
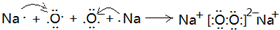
;离子键和非极性键(或离子键和共价键);
(4)化合物C是氯化铝,将化合物氯化铵与化合物氯化铝等物质的量溶于水中,向其中滴加过量的2mol?L-1氢氧化钠溶液,直至形成透明溶液铝离子先和氢氧化钠反应生成氢氧化铝沉淀,然后是铵根离子和氢氧根之间的反应,最后是氢氧化铝溶解的过程,故答案为:Al3++3OH-=Al(OH)3;NH4++OH-=NH3+H2O(NH3?H2O);Al(OH)3+OH-=AlO2-+H2O;
(5)含有钠元素的化合物的检验可以采用颜色反应的方法,颜色反应为黄色,故答案为:焰色反应;火焰呈现黄色.
本题解析:
本题难度:一般
2、选择题 下列陈述I、II正确并且有因果关系的是:
选项
| 陈述I
| 陈述II
|
A
| 常温下铁与浓硫酸、浓硝酸均不反应
| 可用铁槽车密封运送浓硫酸、浓硝酸
|
B
| H2O2、SO2都能使酸性KMnO4褪色
| H2O2表现还原性,SO2表现漂白性
|
C
| Al有还原性
| 利用铝热反应冶炼金属Mn
|
D
| 将水蒸气通过灼热的铁粉,铁粉变红褐色
| 铁粉与水蒸气反应生成Fe2O3
|
?
参考答案:C
本题解析:A、常温下铁与浓硫酸、浓硝酸发生钝化,阻止了铝反应的进行,错误;B、H2O2、SO2都能使酸性KMnO4褪色,二者都表现还原性,错误;C、铝具有还原性,常用来冶炼金属,正确;D、水蒸气与铁反应生成黑色的四氧化三铁,错误,答案选C。
本题难度:一般
3、选择题 X、Y、Z、W、E为原子序数相邻且依次递增的同一短周期元素(稀有气体除外),下列说法正确的是( )
A.若Y为非金属,则X一定为金属
B.Z的氧化物常温下可能为液态
C.X、E的简单离子的半径大小为X>E
D.若E的最高价氧化物对应的水化物的化学式为HmEOn,则其气态氢化物的化学式为H8-2n+mE或EH8-2n+m(m、n均为正整数)
参考答案:A.若Y为非金属,则X可能为B元素,为非金属元素,故A错误;
B.氧化物常温下为液态的只有水,Z肯定不是H元素,则Z的氧化物常温下肯定不是液态,故B错误;
C.当X为金属元素,E为非金属元素,X的离子半径小于E的离子半径,故C错误;
D.若E的最高价氧化物对应的水化物的化学式为HmEOn,E的化合价为2n-m,则氢化物中E的化合价为-(8-2n+m),其气态氢化物的化学式为H8-2n+mE或EH8-2n+m,故D正确.
故选D.
本题解析:
本题难度:简单
4、选择题 根据元素F、S、Cl在周期表中的位置,关于F、S、Cl的说法正确的是( )
A.非金属性:F>S>Cl
B.原子半径:Cl>S>F
C.稳定性:HF>HCl>H2S
D.酸性:HClO4>H2SO4
参考答案:A.F、Cl同主族,S、Cl同周期,则非金属性F>Cl>S,故A错误;
B.F、Cl同主族,S、Cl同周期,则原子半径为S>Cl>F,故B错误;
C.非金属性F>Cl>S,则稳定性为HF>HCl>H2S,故C正确;
D.非金属性Cl>S,则最高价氧化物的水化物的酸性为HClO4>H2SO4,故D正确;
故选CD.
本题解析:
本题难度:一般
5、填空题 已知X和Y两元素的阳离子具有相同的电子层结构,Y元素的阳离子半径比X元素的阳离子半径小。Z和Y两元素原子的电子层数相同,Z元素的原子半径小于Y元素的原子半径。X、Y、Z三种元素原子序数的大小关系是_________________。
参考答案:X<Y<Z
本题解析:
本题难度:一般