1、选择题 下列变化中,吸收的热量用于克服分子间作用力的是( )
A.加热氯化钠晶体使之熔化
B.液氨受热蒸发
C.加热碘化氢气体使之分解
D.加热硅晶体使之熔化
参考答案:A、氯化钠晶体是离子晶体,微粒间的作用力是离子键,故A错误.
B、液氨受热蒸发,克服的是分子间作用力,故B正确.
C、碘化氢分解,发生化学键的断裂,克服的是共价键,故C错误.
D、硅晶体中原子间是共价键,加热硅晶体使之熔化克服的是共价键,故D错误.
故选B.
本题解析:
本题难度:简单
2、填空题 (9分)“西气东输”是西部开发的重点工程,这里的“气”是指天然气,其主要成分是甲烷。水煤气中主要成分是CO和H2,二者的体积比为l :l。已知:在120℃和一个大气压下,H-H键能为436 kJ/mol,O=O键能为496 kJ/mol,H-O键能为463 kJ/mol ;1 mol CO气体完全燃烧生成CO2气体放出283 kJ热量;l mol CH4气体完全燃烧生成CO2气体和气态水放出802 kJ热量。
(1)写出120℃和一个大气压下,H2完全燃烧生成气态水的热化学方程式?;
(2)相同条件下,若l mol CH4气体完全燃烧生成CO2气体和液态水,放出的热量?802 kJ;(选填“>”、“=”、“<”)
(3)忽略水煤气中其他成分,燃烧等体积的CH4和水煤气,所得热量之比约为?;
(4)请结合以上计算结果,叙述相比于水煤气,天然气作为燃料的两个优点:
?。
参考答案:(9分)
(1)2H2(g)+O2(g) = 2H2O(g)?△H= ―484kJ・mol-1(3分,也可分数表示)
(2)>;(2分)
(3) 3.06(3.1)∶1 (2分)?(列式正确均给分如:802:(283+242)/2)
(4)燃烧等体积的气体产生的热量多;产生等量的热量CO2排放量少;CO有毒;以天然气代替水煤气有利于保护环境。(2分,答对2点即可,只答1点给1分,合理答案均给分)
本题解析:略
本题难度:简单
3、选择题 下列说法正确的是? ( )
A.任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同
B.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH相同
C.已知:①2H2(g)+O2(g)=2H2O(g) ΔH=-a kJ・mol-1,②2H2(g)+O2(g)=2H2O(l) ΔH=-b kJ・mol-1,则a>b
D.已知:①C(s,石墨)+O2(g)=CO2(g) ΔH=-393.5 kJ・mol-1,②C(s,金刚石)+O2(g)=CO2(g) ΔH=-395.0 kJ・mol-1,则C(s,石墨)=C(s,金刚石) ΔH=+1.5 kJ・mol-1
参考答案:BD
本题解析:浓酸、弱酸等发生酸碱中和时中和热不同;生成液态水放出更多,故-b<-a,即b>a。反应热大小与条件无关,D项利用盖斯定律可求算。
本题难度:一般
4、选择题 下列说法正确的是?(?)
①用25mL酸式滴定管可以准确放出8.00mL的稀盐酸;
②可用干燥的pH试纸测定氯水的pH;
③使用容量瓶配制溶液,定容时俯视,所得溶液的浓度偏大;
④加入盐酸有使澄清石灰水变浑浊的无色气体生成,则原溶液中一定有大量CO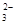 存在;
存在;
⑤在某温度下,醋酸与氢氧化钠溶液混合,溶液呈碱性,溶液中离子浓度大小的关系一定为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+);
⑥右图是反应物和生成物的能量示意图,其可能发生反应的热化学方程式:2A(g)+B(g) 2C(g)? △H=QkJ・mol-1(Q<0)
2C(g)? △H=QkJ・mol-1(Q<0)

A.①③⑥
B.②④⑤
C.①③④
D.③⑤⑥
参考答案:A
本题解析:②错,氯水具有酸性、强氧化性、漂白性等,不可用PH试纸测定氯水的PH值;④错,加入盐酸有使澄清石灰水变浑浊的无色气体生成,则原溶液中可能有CO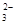 或HCO3―存在;⑤错,可以为氢氧化钠大大过量,即c(Na+)>c(OH-)>c(CH3COO-)>c(H+);
或HCO3―存在;⑤错,可以为氢氧化钠大大过量,即c(Na+)>c(OH-)>c(CH3COO-)>c(H+);
本题难度:一般
5、填空题 (共18分)I(6分)写出下列热化学反应方程式
(1)N2 (g)与H2(g)反应生成1molNH3(g),放出46.1KJ热量。
?
(2)1molC2H5OH(l)完全燃烧生成CO2(g)和H2O(l),放出1366.8KJ热量。
?
(3)1molC(石墨)与适量H2O(g)反应吸收131.3KJ热量
?
II.(12分)(1)化学反应中均伴随着能量的变化,化学键的断裂和形成是发生能量变化的主要原因。生成物中化学键形成时会__________能量(填“放出”或“吸收”);如果一个化学反应,化学键断裂时的能量变化大于化学键形成时的能量变化,则该反应属于_________反应; 如果一个化学反应,反应物的总能量和生成物的总能量有如图所示的关系,则该反应属于__________反应。
如果一个化学反应,反应物的总能量和生成物的总能量有如图所示的关系,则该反应属于__________反应。

(2)不同形式的能量可以相互转换,如:化学能和电能、热能之间的相互转换。如图是一个原电池工作原理的示意图。试回答:

①从能量角度看,它属于____________能转化为____________能;
②装置中Zn为____________极。
参考答案:(18分)I(1)1/2N2(g)+3/2H2(g)=NH3(g)?△H=-46.1 kJ・mol-1
(2)C2H5OH(g)+3O2(g)==2CO2(g)+3H2O(l);△H=-1366.8 kJ・mol-1
(3)C(石墨s)+H2O(g)="=" CO(g)+ H2(g);△H=131.3 kJ・mol-1(每空2分)
II(1)放出?吸热?放热?(2)①化学?电?②负?(每空2分)
本题解析:略
本题难度:一般