1、计算题 工业上制硫酸的主要反应如下:
4FeS2+11O2高温2Fe2O3+8SO2 ?2SO2+O2 2SO3
2SO3
SO3+H2O=H2SO4。
用黄铁矿可以制取H2SO4,再用H2SO4可以制取化肥(NH4)2SO4。煅烧含 FeS2 80.0% 的黄铁矿 80.0 t,最终生产出 83.6 t (NH4)2SO4。已知 NH3的利用率为 92.6%,H2SO4的利用率为 95.0%,试求黄铁矿制取H2SO4时的损失率。
参考答案:37.5%
本题解析:首先须搞清 H2SO4的利用率与 FeS2利用率的关系。并排除 NH3利用率的干扰作用。
其次,根据 S 原子守恒找出已知量 FeS2与未知量(NH4)2SO4的关系(设黄铁矿的利用率为x):
FeS2?~? 2H2SO4? ~? 2(NH4)2SO4
120? 264
80.0 t×80.0%×95.0%・x? 83.6 t
x=62.5%
黄铁矿的损失率为:1.00-62.5%=37.5%。
注: (1)原料利用率(或转化率) = 实际投入原料总量(或转化原料量) ×100%
(2)产物产率 = ? ?×100%
?×100%
(3)中间产物的损耗量(或转化率、利用率)都可归为起始原料的损耗量(或转化率、利用率)
(4)元素的损失率=该化合物的损失率
本题难度:一般
2、实验题 某课外学习小组的同学设计了如图的装置,以验证SO?2的氧化性、还原性和漂白性。
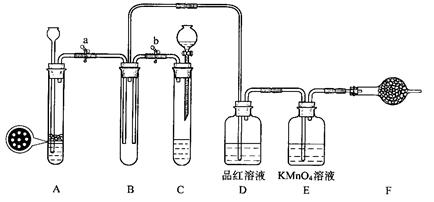
回答以下问题:
33.单独检查装置C的气密性的操作是,关闭活塞b,然后________________________,
若发现________________,说明装置C气密性良好。
34.用Na2SO3固体和硫酸溶液制取SO2气体,应选用__________(选“A”或“C”)做气体发生装置,不选用另一装置的理由是?。
35.小组的同学在A、C装置中的另一个用FeS固体和稀硫酸制取H2S气体,反应的化学方程式为_________________?。
36.SO2气体通过D装置时现象是____________________?,通过E装置时现象是
________________?;SO2与H2S在B装置中反应,现象是______________________。
37.F中盛有碱石灰,其作用是______________________。
参考答案:33.往试管中加水(1分);若水加不进去(1分)
34.C(1分);Na2SO3易溶于水,SO2也易溶于水,不能用有启普发生器功能的装置.(1分,答对1点即可)
35. FeS+H2SO4(稀)à Fe SO4+H2S↑(1分)。
36.红色褪去(1分);紫色褪去(1分); 瓶壁有淡黄色粉末和无色的小液滴(1分,答对1点即可)
37.吸收尾气(1分)
本题解析:33.检查装置C的气密性,关闭活塞b,然后往试管中加水,若水加不进去说明装置C气密性良好。
34.因为Na2SO3是固体粉末,启普发生器隔板盛放不了,和硫酸溶液制取SO2气体,应选用分液漏斗和反应器做气体发生装置。
35.用FeS固体和稀硫酸制取H2S气体为FeS+H2SO4(稀)→ Fe SO4+H2S↑。
36.SO2气体有漂白作用,通过D装置时使品红褪色;SO2气体有还原性,通过E装置时使酸性高锰酸钾溶液褪色;SO2与H2S在B装置中反应:SO2+2H2S→3S+2H2O,瓶壁有淡黄色粉末和无色的小液滴。
37. SO2和H2S都是酸性气体,F中盛有碱石灰,其作用是多余的SO2和H2S。2和H2S气体的发生装置及性质实验设计与评价。
本题难度:一般
3、选择题 下列关于浓硝酸和浓硫酸的叙述正确的是(?)
A.浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
B.浓硝酸具有不稳定性,实验室里应保存在棕色瓶中
C.常温下,浓硝酸可以跟铜缓慢反应,浓硫酸可与铜片迅速反应
D.实验室可以用浓硝酸来制氢气
参考答案:B
本题解析:氨气是碱性气体,不能用浓硫酸来干燥,用碱石灰干燥氨气。常温下铜和浓硫酸不反应,在加热时才能反应。硝酸是氧化性酸和金属反应不能生成氢气。答案选B。
本题难度:一般
4、选择题 下列物质中,有一种物质的漂白作用原理与其余三种不同,这种物质是?
A.漂白粉
B.Na2O2
C.SO2
D.新制氯水
参考答案:C
本题解析:漂白粉含Ca(ClO)2机理和氯水一样,都是利用[O]的漂白作用,SO2则是和色素形成了不稳定化和物。
本题难度:一般
5、选择题 下列化学实验事实及其结论都正确的是
选项
| 实验事实
| 结论
|
A
| 将SO2通入含HClO的溶液中生成H2SO4
| HClO的酸性比H2SO4强
|
B
| 铝箔在酒精灯火焰上加热熔化但不滴落
| 铝箔表面氧化铝熔点高于铝
|
C
| SiO2可以和NaOH溶液及HF溶液反应
| SiO2属于两性氧化性
|
D
| 将SO2通入溴水中,酸性高锰酸钾溶液褪色
| SO2具有漂白性
参考答案:B
本题解析:A、将SO2通入含HClO的溶液中生成H2SO4,主要是HClO的强氧化性氧化SO2;B、正确;C、SiO2只能与HF酸反应与其他酸均不反应,不属两性氧化物;D、SO2使溴水、KMnO4溶液褪色主要是SO2的还原性。2的性质、铝及氧化铝的性质、SiO2的性质等内容。
本题难度:一般
|