1、选择题 对下列化学用语的理解正确的是(? )
A.离子结构示意图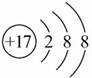 既可以表示35Cl-,也可以表示37Cl-
既可以表示35Cl-,也可以表示37Cl-
B.电子式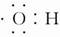 既可以表示羟基,也可以表示氢氧根离子
既可以表示羟基,也可以表示氢氧根离子
C.比例模型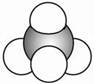 既可以表示甲烷分子,也可以表示四氯化碳分子
既可以表示甲烷分子,也可以表示四氯化碳分子
D.结构简式(CH3)2CHCH3既可以表示正丁烷,也可以表示异丁烷
参考答案:A
本题解析:B项,电子式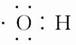 可以表示羟基,氢氧根离子应该表示为
可以表示羟基,氢氧根离子应该表示为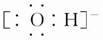 ;C项,比例模型
;C项,比例模型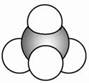 可以表示甲烷分子,但不能表示四氯化碳分子,因为氯原子半径大于碳原子;D项结构简式(CH3)2CHCH3表示异丁烷,正丁烷应该表示为CH3CH2CH2CH3。
可以表示甲烷分子,但不能表示四氯化碳分子,因为氯原子半径大于碳原子;D项结构简式(CH3)2CHCH3表示异丁烷,正丁烷应该表示为CH3CH2CH2CH3。
本题难度:一般
2、选择题 关于如下反应:HgS+O2 ?Hg+SO2,下列叙述不正确的是
?Hg+SO2,下列叙述不正确的是
A.该反应是置换反应
B.该反应转移了4e-
C.Hg是被还原得到的产物
D.HgS既是还原剂又是氧化剂
参考答案:B
本题解析:该反应为置换反应,也一定为氧化还原反应,其中汞元素化合价由+2价降至0价,氧元素由0价降至―2价,而硫元素由―2价升至+4价,故HgS既是还原剂又是氧化剂,反应中转移电子数为6e-,答案为B
本题难度:简单
3、选择题 一定量的乙烷在氧气不足的情况下燃烧,得到CO、CO2和H2O的总质量为55.2g,若将产物通过浓H2SO4,浓H2SO4增重21.6g,则产物中CO的质量为
A.2.8g
B.4. 4g
C.5.6g
D.8.8g
参考答案:A
本题解析:浓H2SO4吸收水蒸气,浓H2SO4增重21.6g,H2O的质量为21.6g,H2O的物质的量为1.2mol,CO和CO2质量为:55.2g-21.6g=33.6g,设CO的物质的量为amol,发生反应方程式并配平:0.4C2H6+O2 aCO+(0.8-a)CO2+1.2H20,可得:a mol * 28g/mol+(0.8-a) mol *44g/mol=33.6g,解得:a="0.1" mol,因此CO的质量为:0.1mol*28g/mol=2.8g。故选A。
aCO+(0.8-a)CO2+1.2H20,可得:a mol * 28g/mol+(0.8-a) mol *44g/mol=33.6g,解得:a="0.1" mol,因此CO的质量为:0.1mol*28g/mol=2.8g。故选A。
点评:根据化学反应的质量守恒来配平本题发生反应的化学方程式的解题的关键,再结合质量是守恒定律。
本题难度:简单
4、选择题 已知下列氧化剂均能氧化+4价的硫元素,为除去稀硫酸中混有的亚硫酸,以得到纯净的稀硫酸,应选用的最合理的氧化剂是(?)
A.KMnO4
B.Ca(ClO)2
C.H2O2
D.Cl2
参考答案:C
本题解析:除去稀硫酸中混有的亚硫酸,以得到纯净的稀硫酸,加入的氧化剂在氧化亚硫酸时,本身被还原的成分为溶液的组成成分。只有H2O2符合题意。反应的方程式为H2O2+H2SO3= H2SO4+H2O。故选项为C。
本题难度:一般
5、选择题 有一钠块放置于潮湿空气中,表面氧化变质,且仍为白色块状固体,称其质量为25g,将其全部投入足量水中反应,得到溶液1000mL,并收集到气体2.24L(标准状况下的纯净物),再取此溶液100mL,用1mol/L的盐酸滴定至中性,用去70mL,并将滴定过程中产生的气体通入到足量的澄清石灰水中,得到干燥的沉淀1g,则金属钠的氧化率为( )
A.18.4%
B.71.4%
C.81.6%
D.28.6%
参考答案:金属钠和水反应生成氢氧化钠和氢气,氧化钠能和水反应生成氢氧化钠,所以收集到气体2.24L全部为氢气,氢气的物质的量n=2.24L22.4L/mol=0.1mol,质量为:0.1mol×2g/mol=0.2g,
设收集到气体2.24L氢气时,消耗金属钠的质量为m,生成氢氧化钠的质量为x,
则? 2Na+2H2O=2NaOH+H2↑?
?46?80? 2
?m?x?0.2g
所以?80x=20.2g? ?46m=20.2g,解得x=8g,m=4.6g,即金属钠的质量是4.6g,即出未被氧化的钠的物质的量为0.2mol,生成氢氧化钠8g,即0.2mol,根据HCl+NaOH=NaCl+H2O,所以得到溶液1000mL中共含有氢氧化钠的物质的量是1mol/L×0.07L×10=0.7mol,或者根据电中性原则,求出取出的100mL溶液中n(Na+)=n(Cl-)=1mol/L×0.07L=0.07mol,则1000mL溶液中n(Na+)=0.7mol,这就是整个钠块中钠的物质的量,故金属钠的氧化率为0.7mol-0.2mol0.7mol×100%=71.4%.
故选B.
本题解析:
本题难度:简单