1、填空题 (18分)目前世界上比较先进的电解制碱技术是离子交换膜法。
(1)在离子交换膜法电解饱和食盐水过程中,与电源正极相联的电极上所发生反应为__________,与电源负极相连的电极附近溶液的pH__________(选填“不变”“升高”“降低”)。
(2)如果粗盐中SO42-含量较高,必须添加试剂除去SO42-,则按添加试剂顺序,依次发生反应的离子方程式为______________________________。
(3)在电解制得的NaOH中往往还含有一定量的NaCl,因此必需进行脱盐工序,脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过__________.冷却.__________(填写操作名称)除去NaCl。
(4)现有阳离子交换膜.阴离子交换膜.石墨电极和如下图所示电解槽,用氯碱工业中的离子交换膜技术原理,可通过电解电解饱和Na2SO4溶液的方法生产NaOH溶液和H2SO4溶液.则电极c为__________极(填“正”.“负”.“阴”.“阳”),b为__________离子交换膜(填“阴”.“阳”)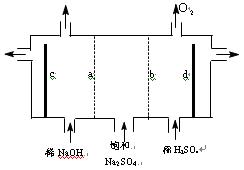
参考答案:(1)2Clˉ-2eˉ="=" Cl2↑(2分)?升高(2分)
(2)Ba2++SO42― = BaSO4↓? CO32―+Ba2+=BaCO3↓? 2H++CO32―= H2O+CO2↑(每个2分,顺序颠倒没分)
(3)蒸发?过滤(每个2分)
(4)阴?阴(每个2分)
本题解析:略
本题难度:一般
2、选择题 1862年一位英国化学家根据O2和Xe的第一电离能非常接近,利用类比思想合成第一种稀有气体化合物,大大推动了对稀有气体的研究,为开拓稀有气体化学作出了历史性的贡献。该化学家为(?)
A.巴尔末
B.巴特列
C.洪特
D.范德华
参考答案:B
本题解析:利用类比思想合成第一种稀有气体化合物的英国化学家是巴特列,所以A项正确;其他化学家在电子排布、分子间作用力等方面做出了贡献。
本题难度:简单
3、选择题 关于石油和煤说法中不正确的是
A.石油是液态烃的混和物,煤是组成复杂的混和物
B.煤的气化液化可制得清洁燃料,减少大气污染
C.直馏汽油、裂化汽油、合成汽油均是石油产品
D.用适当的方法使煤气化,可制得甲烷
参考答案:AC
本题解析:
答案:AC
A、不正确,由不同的碳氢化合物混合组成,其主要组成成分是烷烃,此外石油中还含硫、氧、氮、磷、钒等元素。煤是古代植物经过生物化学作用和地质作用而改变其物理、化学性质,由碳、氢、氧、氮等元素组成的黑色固体矿物。
C、不正确,合成汽油是将石脑油、轻烃、C5、MTBE及助凝助燃添加剂等按照一定比例调和。
本题难度:一般
4、选择题 人工固氮为粮食丰产奠定了基础。下面能实现人工固氮的是?(?)。
A.闪电
B.由氨制硝酸
C.大豆的根瘤
D.合成氨工厂
参考答案:D
本题解析:游离态的氮元素直接转化为氮的化合物的过程是氮的固定,则选项B不是氮的固定;A和C不是人工固氮,答案选D。
点评:该题是主要是考查学生对氮的固定的概念即判断依据的掌握情况,旨在考查学生灵活运用基础知识解决实际问题的能力,难度不大,掌握原理灵活运用即可。
本题难度:简单
5、实验题 农业生产中使用最广泛的磷肥是过磷酸钙,其主要成分是?(填化学式);在实际使用中,其不能与草木灰混合施用的原因是(用离子方程式表示)?。目前常用的湿法磷肥生产工艺是用硫酸分解磷矿石(主要成分为Ca5(PO4)3F),这样处理的主要目的是?。
该生产工艺的有关反应为:
2Ca5(PO4)3F+7H2SO4=Ca3(PO4)2+4H3PO4+7CaSO4+2HF
Ca3(PO4)2+4H3PO4=3Ca(H2PO4)2
生成的氟化氢会和磷矿中带入的二氧化硅反应生成SiF4,若直接排放到空气中,将严重污染环境。某磷肥厂改进工艺,在吸收塔中将SiF4经水吸收后转化为氟硅酸(H2SiF6)溶液和硅胶(SiO2),实现氟的循环使用和硅胶的合理利用,以减小对环境的污染,同时创造经济效益。工艺流程如下:
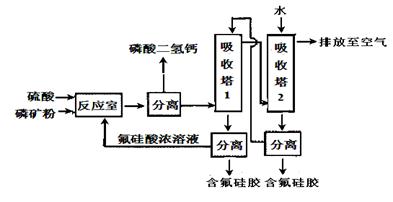
(1)写出吸收塔中反应的化学方程式____?。
(2)该工艺流程中,设计两个吸收塔的目的是?。
(3)氟硅酸与磷酸钙和水反应可生成磷酸二氢钙,原理是:
2H2SiF6+Ca3(PO4)2+4H2O=2CaSiF6・2H20 +Ca(H2PO4)2
CaSiF6・2H2O+2H2O=CaF2・SiO2・2H2O+4HF
4HF+Ca3(PO4)2=2CaF2+Ca(H2PO4)2
若利用氟硅酸与磷酸钙和水反应代替硫酸与磷酸钙反应生产Ca(H2PO4)2,理论上lkg氟硅酸可替代_____kg硫酸。
(4)分离得到的硅胶中因含有H2SiF6而称含氟硅胶,含氟硅胶中SiO2易溶于沸腾的氟化铵溶液,得到(NH4)2SiF6溶液,此反应为可逆反应,加入氨水后,二氧化硅重新析出。写出SiO2与氟化铵反应的化学方程式______?__。
参考答案:(15分)
Ca(H2PO4)2・H2O和CaSO4 (2分); CO32-+H2PO4-+Ca2+=CaHPO4+HCO3-(2分);
使之变为植物可以吸收可溶性的磷酸盐,便于植物吸收(2分)
(1)3SiF4+2H2O=2H2SiF6+SiO2(2分)
(2)提高SiF4R的吸收率(2分)
(3)2.04(2分)
(4)6NH4F(沸腾)+SiO2=(NH4)2SiF6+4NH3+2H2O(3分)
本题解析:K2 CO3和Ca(H2PO4)2反应符合强酸制弱酸原理。Ca5(PO4)3F和 Ca3(PO4)2 不溶,Ca(H2PO4)2可溶。
(3)①2H2SiF6+Ca3(PO4)2+4H2O=2CaSiF6・2H20 +Ca(H2PO4)2
②CaSiF6・2H2O+2H2O=CaF2・SiO2・2H2O+4HF
③4HF+Ca3(PO4)2=2CaF2+Ca(H2PO4)2?
①+②*2+ ③*2?可得关系?2H2SiF6→3Ca(H2PO4)2
④2H2SO4+Ca3(PO4)2="2" CaSO4+ Ca(H2PO4)2?可得关系: 2H2SO4→Ca(H2PO4)2
综合以上两种关系:2H2SiF6→3Ca(H2PO4)2→6H2SO4?设lkg氟硅酸可替代硫酸质量为x。
2*144? 6*98
1? x? x=2.04
本题难度:困难