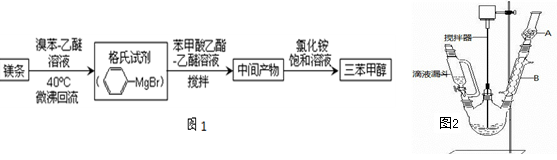
1、实验题 三苯甲醇( )是一种重要的化工原料和医药中间体,实验室合成三苯甲醇其合成流程如图1所示,装置如图2所示。
)是一种重要的化工原料和医药中间体,实验室合成三苯甲醇其合成流程如图1所示,装置如图2所示。
已知:(Ⅰ)格氏试剂容易水解,
 ?(碱式溴化镁);
?(碱式溴化镁);
(Ⅱ)相关物质的物理性质如下:
物质
| 熔点
| 沸点
| 溶解性
|
三苯甲醇
| 164.2℃
| 380℃
| 不溶于水,溶于乙醇、乙醚等有机溶剂
|
乙醚
| -116.3℃
| 34.6℃
| 微溶于水,溶于乙醇、苯等有机溶剂
|
溴苯
| -30.7°C
| 156.2°C
| 不溶于水,溶于乙醇、乙醚等多数有机溶剂
|
苯甲酸乙酯
| -34.6°C
| 212.6°C
| 不溶于水
|
Mg(OH)Br
| 常温下为固体
| 能溶于水,不溶于醇、醚等有机溶剂
|
?
(Ⅲ)三苯甲醇的分子量是260,纯净固体有机物一般都有固定熔点。
请回答以下问题:
(1)图2中玻璃仪器B的名称:?;装有无水CaCl2的仪器A的作用是?;
(2)图2中滴加液体未用普通分液漏斗而用滴液漏斗的作用是?;制取格氏试剂时要保持微沸,可以采用?(方式)加热,优点是?;
(3)制得的三苯甲醇粗产品中,含有乙醚、溴苯、苯甲酸乙酯等有机物和碱式溴化镁等杂质,可以设计如下提纯方案,请填写如下空白:
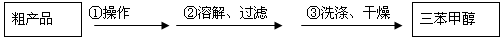
其中,①操作为:?;洗涤液最好选用:?(从选项中选);
A、水? B、乙醚? C、乙醇? D、苯
检验产品已经洗涤干净的操作为:?。
(4)纯度测定:称取2.60g产品,配成乙醚溶液,加入足量金属钠(乙醚与钠不会反应),充分反应后,测得生成气体体积为100.80ml标准状况)。产品中三苯甲醇质量分数为?(保留两位有效数字)。
2、填空题 工业上用铝土矿(主要成分为A12O3,还有少量的Fe2O3,SiO2等杂质)提取氧化铝作冶炼铝的原料,提取的操作过程如下:
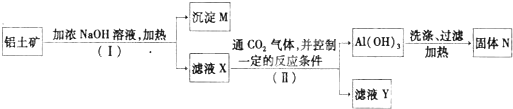
(1)I和II步骤中分离溶液和沉淀的操作是:____________
(2)沉淀M中除含有泥沙外,一定还含有______,固体N是______;
(3)滤液X中,含铝元素的溶质的化学式为______,它属于______(填“酸”、“碱”或“盐”)类物质;写出Ⅰ过程所发生反应的化学方程式______;
(4)实验室里常往AICl3溶液中加人______(填“氨水”或“NaOH溶液”)来制取A1(OH)3,写出该反应的化学方程式______.
3、选择题 下列实验操作不正确的是( )
A.分液时,上层液体上口出,下层液体下口出
B.蒸馏烧瓶内液体的体积不超过其容积的
就可以
C.当蒸发到剩有少量液体时,停止加热,利用余热将液体蒸干
D.过滤时,不能用玻璃棒搅拌漏斗内的待过滤的液体
4、选择题 下列实验操作中叙述不正确的是( )
A.萃取操作必须在分液漏斗中进行
B.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
C.容量瓶用蒸馏水荡洗后不烘干就使用
D.为了便于操作,浓溶液稀释或固体溶解可直接在容量瓶中进行
5、填空题 某盐的无色溶液中同时有Cl-、SO42-,检验时,应先检验?离子,首先取少量待测液于试管中,向其中加入试剂??且至??时,经过?操作后,再用试剂?检验另一种离子。