1、填空题 化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)目前常用的镍(Ni)镉(Cd)电池,其电池总反应式可以表示为:
已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法正确的是____。
①以上反应是可逆反应
②以上反应不是可逆反应
③充电时化学能转变为电能
④放电时化学能转变为电能
A.①③
B.②④
C.①④
D.②③
(2)废弃的镍镉电池已成为主要的环境污染物,有资料表明一节废镍镉电池可以使一平方米面积的耕地失去使用价值。在酸性土壤中这种污染尤为严重。这是因为______________________________________。
参考答案:(1)B
(2)Ni(OH)2和Cd(OH)2能溶于酸性溶液,形成离子,易被植物吸收
本题解析:
本题难度:一般
2、填空题 铅蓄电池是生活中常用的可充电电池,其充电过程与放电过程是完全相反的两个过程。电池总反应为:
? ,请回答下列问题:
,请回答下列问题:
(1)放电时,给出电子的一极发生______反应,其电极反应式为_______。该极充电时将发生_______反应,充电时_______能转化为_____ 能。
(2)放电时,电解质溶液的密度______(填“增大”、“减小”或“不变”)。
(3)放电时,若有0.4 mol H+被消耗,则外电路转移电子的物质的量为_______。
参考答案:(1)氧化;Pb-2e-+SO42- = PbSO4;还原;电;化学
(2)减小
(3)0.2 mol
本题解析:
本题难度:一般
3、选择题
|
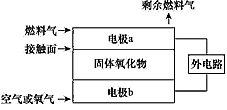
固体氧化物燃料电池(SOFC)以固体氧化物作为电解质,O2-可以在其内部自由通过。其工作原理如图所示。下列关于固体燃料电池的有关说法正确的是
[? ]
A.电极b为电池负极,电极反应式为O2+4e-==2O2-
B.固体氧化物的作用是让电子在电池内通过
C.若H2作为燃料气,则接触面上发生的反应为H2+2OH--4e-==2H++H2O
D.若C2H4作为燃料气,则接触面上发生的反应为C2H4+6O2--12e-==2CO2+2H2O
参考答案:D
本题解析:
本题难度:一般
4、选择题 为体现“城市让生活更美好”的主题,上海市政府承诺世博园区内交通“零排放”、园区周边交通“低排放”。2010年4月15日新能源车交车仪式在世博园举行,该车装着“绿色心脏”――质子交换膜燃料电池,其工作原理如图所示,下列叙述正确的是( )
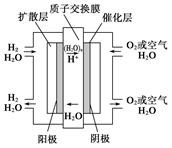
A.通入氧气的电极发生氧化反应
B.通入氢气的电极为正极
C.总反应式为O2+2H2 2H2O
2H2O
D.正极的电极反应式为O2+4H++4e-===2H2O
参考答案:D
本题解析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应,据此可知氢气在负极通入,氧气在正极通入由于氢离子向正极移动,所以正极的电极反应式是O2+4H++4e-===2H2O,选项D正确。A不正确,发生的是还原反应,B不正确,C不正确,反应条件表示点燃,答案选D。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生基础知识的巩固和训练,主要是考查学生对原电池原理的熟悉了解程度,有利于调动学生的学习兴趣和学习积极性,也有助于培养学生的逻辑推理能力。该题的关键是明确原电池的工作原理,然后结合题意灵活运用即可。
本题难度:简单
5、选择题 最新研制的一种由甲醇和氧气以及强碱作电解质溶液的新型手机电池。下列有关此电池的叙述错误的是
[? ]
A.正极电极反应:O2+2H2O+4e-=4OH-
B.负极电极反应:CH3OH+8OH--6e-=CO32-+6H2O
C.电池在使用过程中电解质溶液的pH升高
D.当外电路通过0.6mol电子时,理论上消耗甲醇3.2g
参考答案:C
本题解析:
本题难度:一般