1、选择题 对于3W(g)+2X(g)=4Y(g)+3Z(g),下列反应速率关系正确的是
A.υ(W)=3υ(Z)
B.2υ(X)=3υ(Z)
C.2υ(X)=υ(Y)
D.3υ(W)=2υ(X)
参考答案:C
本题解析:略
本题难度:简单
2、选择题 为探究Fe2+ 对O3氧化I-反应的影响,某研究小组测定两组实验中I3-浓度和体系pH,结果见以下图表。

下列说法不正确的是(? )?
A.在溶液中存在化学平衡I2(aq) + I-(aq)  I3-(aq),其平衡常数表达式为
I3-(aq),其平衡常数表达式为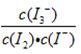
B.第2组实验进行18s后,由于I2(g)不断生成导致I3-浓度下降。
C.3-18s内第2组实验中生成I3-的平均反应速率约为0.55 mol/(L・s)
D.Fe2+可作为O3氧化I-的催化剂
参考答案:C
本题解析:因平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,所以K= ,A选项正确;c(Fe3+)增加,发生反应:2Fe3++2I-=I2+2Fe2+,消耗I-,I2(g)不断生成,都会使I2(aq)+I-(aq)
,A选项正确;c(Fe3+)增加,发生反应:2Fe3++2I-=I2+2Fe2+,消耗I-,I2(g)不断生成,都会使I2(aq)+I-(aq) I3-(aq)平衡逆向移动,使c(I3-)急剧减小,B选项正确;3-18s内第2组实验中生成I3-的平均反应速率约为
I3-(aq)平衡逆向移动,使c(I3-)急剧减小,B选项正确;3-18s内第2组实验中生成I3-的平均反应速率约为 =0.55×10-3 mol/(L・s),C选项错误;由于是持续通入O3,O3可以将Fe2+氧化为Fe3+:O3+2Fe2++2H+=2Fe3++O2+H2O,Fe3+氧化I-:2Fe3++2I-=I2+2Fe2+,所以Fe2+可看作为O3氧化I-的催化剂,D选项正确。
=0.55×10-3 mol/(L・s),C选项错误;由于是持续通入O3,O3可以将Fe2+氧化为Fe3+:O3+2Fe2++2H+=2Fe3++O2+H2O,Fe3+氧化I-:2Fe3++2I-=I2+2Fe2+,所以Fe2+可看作为O3氧化I-的催化剂,D选项正确。
本题难度:一般
3、填空题 (6分)对于反应2N(g)+3 M(g) XQ(g)+3R(g),在容积为4L的密闭容器中,将2mol气体N和3mol气体M混合,当反应经2min后
XQ(g)+3R(g),在容积为4L的密闭容器中,将2mol气体N和3mol气体M混合,当反应经2min后 达平衡时生成2.4 mol气体R,并测得Q的浓度为0.4mol/L,则X的值为 ,M的转化率为 ,用M物质表示的反应速率vM=
达平衡时生成2.4 mol气体R,并测得Q的浓度为0.4mol/L,则X的值为 ,M的转化率为 ,用M物质表示的反应速率vM=
参考答案: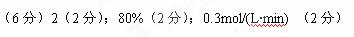
本题解析:略
本题难度:一般
4、选择题 下列反应中生成H2的速率最快的是
| 金属
| 酸溶液
| 温度
|
A
| Mg
| 0.5mol?L-1H2SO4
| 20℃
|
B
| Fe
| 1 mol?L-1HCl
| 20℃
|
C
| Zn
| 2 mol?L-1HCl
| 30℃
|
D
| Mg
| 1 mol?L-1H2SO4
| 30℃
|
参考答案:D
本题解析:考查外界条件对反应速率的影响。在其它条件不变的情况下,增多反应物浓度或升高温度或增大反应物的接触面积或使用催化剂均能加快反应速率。同时反应物本身的性质也是决定性因素,镁最活泼,和酸反应最剧烈,所以选项D是正确的,答案选D。
本题难度:一般
5、选择题 下列对化学反应速率影响因素的分析错误的是( )
A.一定浓度稀硫酸与过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量K2SO4溶液
B.NO+CO2

NO2+CO在密闭容器中进行,压强不变充入N2使体积增大,反应速率不变
C.升高温度时,化学反应速率加快,主要是由于反应物分子的能量增加,活化分子百分数增大,有效
碰撞次数增多,化学反应速率加快
D.催化剂能改变化学反应速率且参与反应,但催化剂在化学反应前后,化学性质和质量都不变
参考答案:A、锌和酸的反应中,向反应物中加入适量K2SO4溶液相当于加入一定量的水,则酸的浓度会降低,化学反应速率减慢,由于氢离子的物质的量不变,所以生成氢气的量不变,故A正确;
B、压强不变充入N2使体积增大,相当于降低了各个物质的浓度,反应速率减慢,故B错误;
C、升高温度会使得反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多,化学反应速率加快,故C正确;
D、催化剂能改变化学反应速率且参与反应,在化学反应前后,化学性质和质量都不变,故D正确.
故选B.
本题解析:
本题难度:一般