1、选择题 最外层有2个电子的主族元素X与最外层有7个电子的另一主族元素Y化合,以下有关描述错误的是( )
A.X与Y可形成XY2型离子化合物
B.在XY2中X的原子半径比Y原子半径大
C.在形成化合物XY2时,X元素被氧化而Y元素被还原
D.生成化合物一定溶于水
参考答案:BD
本题解析:X的一个原子失去两个电子变成X2+,Y的一个原子获得一个电子变成Y-,二者相互作用可形成XY2型离子化合物;A项正确,不是答案。在XY2型离子化合物中,X的原子半径不一定比Y的半径大,如MgBr2中,镁离子的半径就小于溴离子半径;B项不正确。在形成化合物XY2时,X元素的原子失去电子被氧化,而Y元素的原子得到电子被还原;C项正确,不是答案。离子化合物不一定都溶于水,如CaF2就不溶于水,D不正确。本题要求找出错误的描述,故B、D应为答案。
本题难度:一般
2、填空题 (8分)下表表示的是元素周期表中短周期元素,根据要求回答下列问题:
(1)④⑥元素气态氢化物的稳定性比较?> ?(写化学式)(2分)
(2)③号元素与其他元素可形成10个电子的阳离子和阴离子,其离子符号分别为?、?。(2分)
(3)用电子式表示⑧和③元素形成A2B型化合物的过程。(2分)
?
(4)用电子式表示⑤和⑥元素形成A2B型化合物的过程。(2分)
?
参考答案:(1)HF>H2S (2分)(2)H3O+? OH-?(2分)
(3)?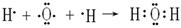 ?(2分)
?(2分)
(4)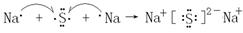 ?(2分)
?(2分)
本题解析:略
本题难度:简单
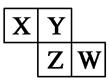
3、选择题 X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示。若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( ? )
A.X的最常见气态氢化物的水溶液显酸性
B.最高价氧化物对应水化物的酸性W比Z强
C.Z的单质与氢气反应较W剧烈
D.X的原子半径小于Y
参考答案:B
本题解析:X、Y、Z、W均为短周期元素,Z原子的最外层电子数是第一层电子数的3倍,则Z的第一层电子数为2,最外层电子数为6,所以Z应为S,结合位置可知,Y为O,X为N,W为Cl,A、X的最常见气态氢化物为氨气,其水溶液显碱性,错误;B、非金属性Cl>S,则最高价氧化物对应水化物的酸性W比Z强,正确;C、非金属性Cl>S,则W的单质与氢气反应较Z剧烈,错误;D、同周期从左至右原子半径减小,则X的原子半径大于Y,错误。
本题难度:简单
4、填空题 (10分)有A、B、C、D、E五种短周期元素,它们的核电荷数按C、A、B、D、E
的顺序增大。C、D都能分别与A按原子个数比为1∶1或2∶1形成化合物;CB可与EA2
反应生成C2A和气态物质EB4;E的M层电子数是K层电子数的2倍。
(1)写出下列元素的名称:A_______,B_______, E_______。
(2)画出E的原子结构示意图_____?__。
写出电子式D2A2___?____,EB4__?_?____。
(3)比较EA2与EB4的熔点高低(填化学式)_______>_______。
(4)A的氢化物的沸点与同族下一周期元素的氢化物相比,A的氢化物的沸点?(填“高”或“低”),原因是?。
参考答案:(1)氧、氟、硅(2)略(3)SiO2;SiF4(4)高,因为A的氢化物分子间可形成氢键,而另一种则无。(每空1分共10分)
本题解析:略
本题难度:简单
5、选择题 月球含有丰富的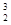 He。下列关于
He。下列关于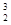 He的说法不正确的是? ( )
He的说法不正确的是? ( )
A.核外电子排布为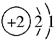
B.原子核内有1个中子
C.与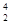 He互为同位素
He互为同位素
D.比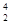 He具有相同的质子数
He具有相同的质子数
参考答案:A
本题解析: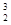 He和
He和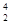 He的核外电子数相等,都为2。
He的核外电子数相等,都为2。
本题难度:一般