1��ʵ���� ��8�֣�50 mL1.0 mol��L��1�����50mL1.1 mol��L��1����������Һ����ͼװ���н����кͷ�Ӧ��ͨ���� ����Ӧ���������ų��������ɼ����к��ȡ��Իش��������⡣
����Ӧ���������ų��������ɼ����к��ȡ��Իش��������⡣
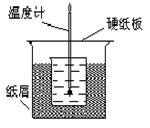
�Ŵ�С�ձ���������ֽ����������ʲô��
�ƴ��ձ����粻��Ӳֽ�壬������к��ȵ���ֵ�к�Ӱ��?
�Ǹ���60 mL1.0mol��L��1�����50mL1.1mol��L��1����������Һ���з�Ӧ��������ʵ����ȣ������к��ȵ���ֵ�������Ƿ���ȣ������ǿ�����Ӱ�죩���������ɡ�
������ͬŨ�Ⱥ�����İ�ˮ����NaOH��Һ����ʵ�飬Ϊʲô����к��ȵ���ֵƫ�ͣ�
2������� (9��)����P(s)��Cl2 (g)������Ӧ����PCl3(g)��PCl5(g)����Ӧ���̺�������ϵ��ͼ��ʾ
��ͼ�еĦ�H��ʾ����lmol��������ݣ���

������ͼ�ش��������⣺
��1�� PCl5�ֽ��PCl3 ��Cl2���Ȼ�ѧ����ʽ��________?______��
�����ֽⷴӦ��һ�����淴Ӧ���¶�T1ʱ�����ܱ������м���0.80 mol PC15����Ӧ��ƽ��ʱPC15��ʣ0.60 mol����ֽ�����1����________������Ӧ�¶���Tl���ߵ�T2��ƽ��ʱPC15�ķֽ�����2Ϊ����2_______��1������ڡ�����С�ڡ����ڡ�) ��
��2����ҵ���Ʊ�PCl5ͨ�����������У��Ƚ�P��Cl2��Ӧ�����м����PCl3��Ȼ���£��ٺ�Cl2��Ӧ����PCl5ԭ����_______________________________________________
��3��P��Cl2��������Ӧ����1molPCl5�Ħ�H3����_____________________��P��Cl2һ����Ӧ����1 mol PCl5�Ħ�H4___________��H3��������ڡ�����С�ڡ����ڡ���
3������� ��һ�������£�1 molij��������O2��ȫ��������98.0 kJ������2 mol��������1 mol O2�ڴ������·�����Ӧ���ﵽƽ��ʱ�ų���������176.4 kJ����������ת����Ϊ��������?��
��ע��ij��Ӧ���ת����=�÷�Ӧ��ת��(����)�����ʵ����¸÷�Ӧ����ʼ�����ʵ�����100%��
4��ѡ���� ��֪�Ȼ�ѧ����ʽ��SO2(g)+ 1/2O2(g)  ?SO3(g)?��H = �D98.32kJ��mol���������г���2molSO2?��1molO2��ַ�Ӧ�����շų�������Ϊ
?SO3(g)?��H = �D98.32kJ��mol���������г���2molSO2?��1molO2��ַ�Ӧ�����շų�������Ϊ
A��196.64kJ
B��196.64kJ��mol
C����196.64kJ
D����196.64kJ
5��ѡ���� �����й������仯˵����ȷ���ǣ�?����
A����ѧ��Ӧ���������������⣬�������������ı仯
B�����ȷ�Ӧ������Ҫ���ȾͿ��Է���
C����Ҫ���ȵĻ�ѧ��Ӧ�������ȷ�Ӧ
D����ѧ��Ӧ���Ȼ������ȣ�ȡ���ڷ�Ӧ����