|
高中化学知识点归纳《化学平衡》高频考点强化练习(2019年最新版)(十)
2020-08-13 06:49:41
【 大 中 小】
|
1、选择题 在密闭容器中,反应xA(g)  yB(g)达到平衡后,保持温度不变,将容器体积增加为原来的二倍,当达到新的平衡时,B的浓度是原来的70%,则 yB(g)达到平衡后,保持温度不变,将容器体积增加为原来的二倍,当达到新的平衡时,B的浓度是原来的70%,则
A.平衡向正反应方向移动了
B.物质A的转化率减少了
C.物质B的质量分数减少了
D.x>y
|
参考答案:A
本题解析:保持温度不变,将容器体积增加为原来的二倍,如果平衡不移动,B的浓度是原来的50%,实际上,当达到新的平衡时,B的浓度是原来的70%,说明平衡向正反应方向移动,物质A的转化率增大了,物质B的质量分数增大,而减小压强,平衡向系数增大的方向移动,即x<y,选A。
考点:考查影响化学平衡的因素。
本题难度:一般
2、填空题 已知,常温下1体积水能溶解2体积氯气,并且氯水中有如下平衡:Cl2 + H2O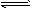 HCl + HClO HCl + HClO
(1)常温下,在一个体积为100mL的透明玻璃针筒里吸入80mL氯气后,再吸进10mL水,振荡后静置。写出针筒中观察到的现象是_____________________。
(2)将上述针筒长时间放置,又能看到何种变化__________;试用平衡观点加以解释__________。
参考答案:(1)气体体积缩小,溶液呈浅黄绿色
(2)气体体积继续减小(至约40 mL),气体和溶液的颜色均逐渐变浅(直至无色);氯水中存在平衡
Cl2 + H2O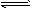 HCl + HClO,由于2HClO == 2HCl + O2↑,HClO不断分解,使上述平衡右移,最终Cl2耗尽全部转化为O2,由总关系式为:2Cl2~O2 HCl + HClO,由于2HClO == 2HCl + O2↑,HClO不断分解,使上述平衡右移,最终Cl2耗尽全部转化为O2,由总关系式为:2Cl2~O2
本题解析:
本题难度:一般
3、填空题 可逆反应3A(g) 3B(?)+C(?)(正反应吸热)达到化学平衡后, 3B(?)+C(?)(正反应吸热)达到化学平衡后,
(1)升高温度,用“变大”、“变小”、“不变”或“无法确定”填空。
①若B、C都是气体,气体的平均相对分子质量 ;
②若B、C都不是气体,气体的平均相对分子质量 ;
③若B是气体,C不是气体,气体的平均相对分子质量 ;
(2)如果平衡后保持温度不变,将容器体积增加一倍,新平衡时A的浓度是原来的60%,则B是 态,C是 态。
(3)如果B为气体,C为固体,取3molA恒温下在1L容器中充分反应,平衡时测得B的浓度为2.1mol/L。若使反应从逆反应开始,起始时在容器中加入3molB ,同样条件下,要使平衡时B的浓度仍为2.1mol/L,则C的取值范围应该是 。
参考答案:(1)变小 不变 变小 (2)固体或液体 固体或液体或气体 (3) C(C)>0.3mol
本题解析:(1)可逆反应3A(g) 3B(?)+C(?)(正反应吸热),所以当温度升高,平衡向正反应方向进行,①若B、C都是气体,则正反应方向为分子数增加的反应,故气体的平均相对分子质量增加;②若B、C都不是气体,则气体就只有A,所以气体的平均相对分子质量不变;③若B是气体,C不是气体,则该反应的气体的分子数不变,但是C为非气体,故气态物质的质量比原理减小了,所以气体的平均相对分子质量变小;(2)如果平衡后保持温度不变,将容器体积增加一倍,此时A的浓度必须为原来的50%,但是达到新平衡时A的浓度是原来的60%,说明了反应向逆反应方向移动,所以B为固体或液体,而C可以为 固体或液体或气体;(3)B为气体,C为固体,说明了只要C足量,压强对该反应是没有影响的,3molA恒温下在1L容器中充分反应,平衡时测得B的浓度为2.1mol/L,则消耗的A为2.1mol,剩下0.9molA,而使反应从逆反应开始,起始时在容器中加入3molB ,同样条件下,要使平衡时B的浓度仍为2.1mol/L,即B为2.1mol,要生产0.9molA,需要0.3molC,所以C的物质的量要大于0.3mol。 3B(?)+C(?)(正反应吸热),所以当温度升高,平衡向正反应方向进行,①若B、C都是气体,则正反应方向为分子数增加的反应,故气体的平均相对分子质量增加;②若B、C都不是气体,则气体就只有A,所以气体的平均相对分子质量不变;③若B是气体,C不是气体,则该反应的气体的分子数不变,但是C为非气体,故气态物质的质量比原理减小了,所以气体的平均相对分子质量变小;(2)如果平衡后保持温度不变,将容器体积增加一倍,此时A的浓度必须为原来的50%,但是达到新平衡时A的浓度是原来的60%,说明了反应向逆反应方向移动,所以B为固体或液体,而C可以为 固体或液体或气体;(3)B为气体,C为固体,说明了只要C足量,压强对该反应是没有影响的,3molA恒温下在1L容器中充分反应,平衡时测得B的浓度为2.1mol/L,则消耗的A为2.1mol,剩下0.9molA,而使反应从逆反应开始,起始时在容器中加入3molB ,同样条件下,要使平衡时B的浓度仍为2.1mol/L,即B为2.1mol,要生产0.9molA,需要0.3molC,所以C的物质的量要大于0.3mol。
考点:影响化学平衡的因素
点评:本题考查了影响化学平衡的因素,该考点是高考考查的重点和难点,本题综合性好,对学生的分析能量要求比较高,该题有一定的难度。
本题难度:困难
4、填空题 已知反应:aA(g)+bB(g)?cC(g)
根据图形推测:
(1)P1______P2?(?填>或<)
(2)a+b______c?(?填>或<)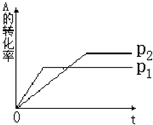
参考答案:(1)由图象可知P1曲线反应速率较大,说明P1压强较大,故答案为:>;
(2)压强增大,A的转化率减小,说明增大压强,平衡向逆反应方向移动,则有a+b<c,故答案为:<.
本题解析:
本题难度:一般
5、选择题 某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g) 2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据如图可得出的判断结论正确的是 2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据如图可得出的判断结论正确的是
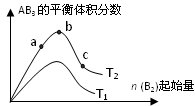
A.反应速率a>b>c
B.若T2>T1,则正反应一定是吸热反应
C.达到平衡时,AB3的物质的量大小为:b > c > a
D.达到平衡时A2的转化率大小为:b>a>c
|