1、选择题 一种新型的燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极通入乙烷和氧气,其总反应为:2C2H6+7O2+8KOH=4K2CO3+10H2O。有关此电池的推断正确的是(?)
A.负极反应为:14H2O+7O2+28e―=28OH―
B.放电一段时间后,负极周围的pH升高
C.理论上消耗1mol C2H6,电路上转移的电子为14mol
D.放电过程中,K+向负极移动
2、填空题 (6分)用铜片、银片、Cu (NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U型管)构成一个原电池。这个原电池的负极是?,电极反应式是?;
正极是?,电极反应式是?。
3、选择题 一种新型酸性乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍,电池反应式为C2H5OH + 3O2 =" 2" CO2 + 3H2O,电池构造如下图。下列关于该电池的说法不正确的是

A.放电过程中,电源内部的H+从正极区向负极区迁移
B.通入乙醇的电极是负极
C.该电池的正极反应为:4H+ + O2 + 4e-= 2H2O
D.用该电池做为电源,用惰性电极电解饱和NaCl的水溶液时,每消耗0.2 mol C2H5OH,阳极产生标准状况下气体的体积为26.88 L
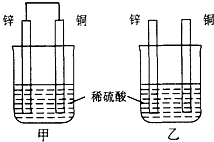
4、简答题 将纯锌片和纯铜片按如图方式插入100ml相同浓度的稀硫酸中一段时间,请回答下列问题:
(1)下列说法正确的是______.
A、甲、乙均为化学能转变为电能的装置
B、乙中铜片上没有明显变化
C、甲中铜片质量减少、乙中锌片质量减少
D、两烧杯中溶液的pH均增大
(2)在相同时间内,两烧杯中产生气泡的速度:甲______乙(填“>”、“<“或“=”).
(3)当甲中产生1.12L(标准状况)气体时,通过导线的电子为______mol.
(4)这时,甲中负极发生氧化反应,溶解了______g.
5、选择题 氢氧燃料电池已用于航天飞机。以30%KOH溶液为电解质的这种电池在使用时的电极反应如下:2H2+4OH--4e- ==4H2O? O2+2H2O+4e-==4OH-下列说法错误的是
A.氢气通入正极,氧气通入负极
B.燃料电池的能量转化率不能达到100%
C.供电时的总反应为:2H2+O2 ="===" 2H2O
D.产物为无污染的水,属于环境友好电池