1、填空题 稀土元素是周期表中ⅢB族钪、钇和镧系元素的总称,它们都是很活泼的金属,性质极为相似,常见化合价为+3。其中钇(Y)元素是激光和超导的重要材料。我国蕴藏着丰富的钇矿石(Y2FeBe2Si2O10),以此矿石为原料生产氧化钇(Y2O3)的主要流程如下

已知:①有关金属离子形成氢氧化物沉淀时的pH如下表
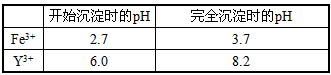
②在周期表中,铍、铝元素处于第二周期和第三周期的对角线位置,化学性质相似。
(1)钇矿石(Y2FeBe2Si2O10)的组成用氧化物的形式可表示为_______________。
(2)欲从Na2SiO3和Na2BeO2的混合溶液中制得Be(OH)2沉淀。则①最好选用盐酸、____(填字母)两种试剂,再通过必要的操作即可实现。
a.NaOH溶液 b.氨水 c.CO2气 d.HNO3
②写出Na2BeO2与足量盐酸发生反应的离子方程式: ______________________。
(3)为使Fe3+沉淀完全,须用氨水调节pH =a,则a应控制在_________的范围内;检验Fe3+是否沉淀完全的操作方法是_______________________
参考答案:(1)Y2O3・FeO・2BeO・2SiO2
(2)①b;②BeO22- + 4H+ = Be2+ +2H2O
(3)3.7~6.0;取少量滤液,滴加几滴KSCN溶液,观察溶液是否变为血红色,若不变血红色,则说明Fe3+
沉淀完全
本题解析:
本题难度:一般
2、填空题 工业上用铜屑和浓硝酸为原料制取硝酸铜。在实际生产中,需把浓硝酸用等体积的水稀释。试简要回答下列问题:
(1)用稀硝酸而不用浓硝酸的原因是___
(2)从经济效益和环境保护角度考虑,设计制取硝酸铜最适宜的方法,用化学方程式表示为____
参考答案:(1)用稀硝酸消耗原料较少,且产生污染物较少
(2)2Cu+O2=2CuO,CuO+2HNO3= Cu(NO3)2+H2O
本题解析:
本题难度:一般
3、选择题 我国许多城市已经推广使用清洁燃料,如压缩天然气(CNG)类和液化石油气(LPG)类.这两类燃料的主要成分是( )
A.醇类
B.一氧化碳
C.氢气
D.烃类
参考答案:D
本题解析:
本题难度:简单
4、填空题 由黄铜矿(主要成分是CuFeS2)炼制精铜的工艺流程示意图如下:

(1)在反射炉中,把铜精矿砂和石英砂混合加热到1000°C左右,黄铜矿与空气反应生成Cu和Fe的低价硫化物,且部分Fe的硫化物转变为低价氧化物,该过程中两个主要反应的化学方程式分别是__________,_________反射炉内生成炉渣的主要成分是____;
(2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%。转炉中,将冰铜加熔剂(石英砂)在1200°C左右吹入空气进行吹炼。冰铜中的Cu2S被氧化成Cu2O,生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式分别是____;
(3)粗铜的电解精炼如图所示。在粗铜的电解过程中,粗铜板应是图中电极____(填图中的字母);在电极d上发生的电极反应式为______;若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为_____。
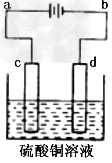
参考答案:(1)2Cu2FeS2+O2 Cu2S+2FeS+?SO2;2FeS+3O2
Cu2S+2FeS+?SO2;2FeS+3O2 2FeO+2SO2;FeSiO3
2FeO+2SO2;FeSiO3
(2)2Cu2S+3O2 2Cu2O+2SO2、2Cu2O+?Cu2S
2Cu2O+2SO2、2Cu2O+?Cu2S 6Cu+?SO2↑
6Cu+?SO2↑
(3)c;Cu2++2e-=Cu;Au、Ag以单质的形式沉积在c(阳极)下方,Fe以Fe2+的形式进入电解液中
本题解析:
本题难度:一般
5、填空题 (三选一)【化学―化学与技术】
碘酸钾是一种白色结晶,无臭无味,酸性条件下碘酸钾是一种较强的氧化剂,与氢碘酸、二氧化硫等还原性物质作用,被还原为单质碘;在碱性介质中,碘酸钾能被氯气、次氯酸盐等氧化为高碘酸钾。碘酸钾在常温下稳定,加热至560?℃开始分解。工业生产碘酸钾的流程如下,在反应器中发生反应的化学方程式为:6I2?+11KClO3?+3H2O=6KH(IO3)2?+?5KCl?+?3Cl2

试回答下列问题:
(1)步骤①反应器发生的反应中,转移电子总数为___________;
(2)步骤②中,用硝酸而不用HI,其原因可能是______________________;
(3)步骤③要保持溶液微沸1小时以完全排出氯气,排出氯气的原因为________;
(4)步骤⑧用氢氧化钾调节溶液的pH,反应的化学方程式为:________;
参考答案:(1)60
(2)HI具有还原性,能将已生成的碘酸氢钾还原
(3)Cl2及Cl2与KOH反应生成的KClO,能将KIO3氧化成KIO4
(4)KH(IO3)2?+?KOH?=?2KIO3?+?H2O
本题解析:
本题难度:一般