1、选择题 实验室做氨的催化氧化试验,不可能产生的物质是…
A.N2
B.NO
C.NO2
D.NH4NO3
参考答案:A
本题解析:氨的催化氧化反应为:4NH3+5O2=4NO+6H2O, 以后根据各量的不同,可能发生以下各反应:
2NO+O2=2NO2,
3NO2+H2O=2HNO3+NO,
NH3+HNO3=NH4NO3,
因此,不可能生成的产物为N2.
本题难度:困难
2、选择题 向lL0.8mol/L硫酸溶液中加入20.2gKNO3和19.2g铜粉,充分反应后产生的气体是 _______ ,在标准状况下的体积为______ 。
A.氢气? 2.24L
B.一氧化氮? 4.48L
C.氢气? 4.48L
D.一氧化氮? 2.24L
参考答案:B
本题解析:酸性条件下,硝酸根离子与金属反应不会产生氢气,A、C错。根据氢离子与硝酸根离子、铜之间反应的离子方程式,可判断出0.2mol硝酸根离子恰好完全反应,所以生成标准状况下NO 0.2mol,即4.48L。
本题难度:困难
3、选择题 取不同质量的镁铝合金分别与25mL同浓度的稀硝酸反应,测量合金的质量与产生气体的体积(标准状况),列表如下:
A.A
B.B
C.C
D.D
参考答案:AD
本题解析:分析:分析1、2组数据可知,金属的质量之比等于对应NO的体积之比,说明1、2组金属完全反应,第3组金属若完全反应,可得NO体积为224mL×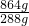 =672mL>560mL,故第3组金属有剩余,硝酸完全反应.
=672mL>560mL,故第3组金属有剩余,硝酸完全反应.
第3个实验后向反应容器内加入足量的1.0mol/L?NaOH(aq)充分反应,使固体质量不再发生变化,使氢氧化铝恰好转化为NaAlO2,需要氢氧化钠溶液的体积最小,此时溶液中溶质为NaNO3、NaAlO2.
根据n=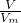 计算第3组生成的NO的物质的量,由反应3Zn+8HNO3=3Zn(NO3)2+2NO↑+4H2O、Al+4HNO3=Al(NO3)3+NO↑+2H2O可知,起氧化剂作用的硝酸为总的硝酸的
计算第3组生成的NO的物质的量,由反应3Zn+8HNO3=3Zn(NO3)2+2NO↑+4H2O、Al+4HNO3=Al(NO3)3+NO↑+2H2O可知,起氧化剂作用的硝酸为总的硝酸的 ,据此计算25mL硝酸溶液中n(HNO3)、起酸性作用的硝酸的物质的量,根据c=
,据此计算25mL硝酸溶液中n(HNO3)、起酸性作用的硝酸的物质的量,根据c=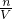 计算原硝酸溶液的浓度;
计算原硝酸溶液的浓度;
令144mg合金中Mg、Al的物质的量分别为xmol、ymol,根据二者质量与转移电子数目列方程计算x、y的值,进而计算864mg合金中Al的物质的量,根据钠离子守恒可知n(NaOH)=n(NaNO3)+n(NaAlO2),再根据V= 计算需要氢氧化钠溶液的最小体积.
计算需要氢氧化钠溶液的最小体积.
解答:分析1、2组数据可知,金属的质量之比等于对应NO的体积之比,说明1、2组金属完全反应,第3组金属若完全反应,可得NO体积为224mL×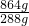 =672mL>560mL,故第3组金属有剩余,硝酸完全反应.
=672mL>560mL,故第3组金属有剩余,硝酸完全反应.
第3个实验后向反应容器内加入足量的1.0mol/L?NaOH(aq)充分反应,使固体质量不再发生变化,使氢氧化铝恰好转化为NaAlO2,需要氢氧化钠溶液的体积最小,此时溶液中溶质为NaNO3、NaAlO2.
第3组生成的NO的物质的量为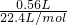 =0.025mol,由反应3Zn+8HNO3=3Zn(NO3)2+2NO↑+4H2O、Al+4HNO3=Al(NO3)3+NO↑+2H2O可知,起氧化剂作用的硝酸为总的硝酸的
=0.025mol,由反应3Zn+8HNO3=3Zn(NO3)2+2NO↑+4H2O、Al+4HNO3=Al(NO3)3+NO↑+2H2O可知,起氧化剂作用的硝酸为总的硝酸的 ,故25mL硝酸溶液中n(HNO3)=0.025mol÷
,故25mL硝酸溶液中n(HNO3)=0.025mol÷
=0.1mol,原硝酸溶液的浓度为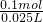 =4mol/L.
=4mol/L.
起酸性作用的硝酸的物质的量为0.1mol-0.025mol=0.075mol,
令144mg合金中Mg、Al的物质的量分别为xmol、ymol,由二者质量与转移电子数目守恒有:
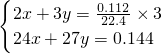
解得x=0.0015,y=0.004,
故864mg合金中Al的物质的量0.004mol×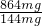 =0.024mol,根据钠离子守恒可知n(NaOH)=n(NaNO3)+n(NaAlO2)=0.075mol+0.024mol=0.099mol,故需要氢氧化钠溶液的最小体积为
=0.024mol,根据钠离子守恒可知n(NaOH)=n(NaNO3)+n(NaAlO2)=0.075mol+0.024mol=0.099mol,故需要氢氧化钠溶液的最小体积为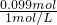 =0.099L=99mL,
=0.099L=99mL,
故选AD.
点评:本题考查混合物的有关计算,过程复杂、计算量较大,题目难度较大,注意利用守恒思想进行的解答.
本题难度:困难
4、选择题  下表各组物质中,物质之间通过一步反应就能实现如图所示转化的是
下表各组物质中,物质之间通过一步反应就能实现如图所示转化的是
A.A
B.B
C.C
D.D
参考答案:D
本题解析:分析:A.Al和NaOH生成NaAlO2而不是Al(OH)3;
B.CH3CH2OH和CH3COOH反应生成乙酸乙酯,不能生成乙醛;
C.NaHCO3与CO2不反应;
C.Cl2和Fe反应生成FeCl3,FeCl3与Fe反应生成FeCl2,Cl2与FeCl2反应生成FeCl3.
解答:A.Al和NaOH生成NaAlO2而不是Al(OH)3,如a为AlCl3可符合,故A错误;
B.CH3CH2OH和CH3COOH反应生成乙酸乙酯,不能生成乙醛,故B错误;
C.NaHCO3与CO2不反应,故C错误;
D.Cl2和Fe反应生成FeCl3,FeCl3与Fe反应生成FeCl2,Cl2与FeCl2反应生成FeCl3,符合转化关系,故D正确.
故选D.
点评:本题考查无机物的推断,题目侧重于元素化合物的考查,注意把握相关物质的性质,题目难度不大.
本题难度:困难
5、选择题 下列离子方程式的表达正确的是
A.CuSO4溶液与Ba(OH)2溶液混合:Ba2++SO42-=BaSO4↓
B.NaHCO3溶液与稀硫酸混合:HCO3-+H+=H2O+CO2↑
C.NaHSO3溶液与NaHSO4溶液混合:HSO3-+HSO4-=SO42-+H2O+SO2↑
D.Ca(OH)2溶液中通入过量CO2:Ca2++2OH-+CO2=CaCO3↓+H2O
参考答案:B
本题解析:分析:A、离子反应不能漏掉反应的离子;
B、碳酸氢根离子和氢离子反应生成水和二氧化碳;
C、亚硫酸氢根离子和氢离子反应生成二氧化硫和水;
D、注意二氧化碳过量时,会将碳酸盐转化为碳酸氢盐.
解答:A、CuSO4溶液与Ba(OH)2溶液混合后的反应实质为:Cu2++2OH-+Ba2++SO42-=BaSO4↓+Cu(OH)2↓,故A错误;
B、NaHCO3溶液与稀硫酸混合后,碳酸氢根离子和氢离子反应生成水和二氧化碳,即:HCO3-+H+=H2O+CO2↑,故B正确;
C、NaHSO4溶液中含有钠离子、硫酸根离子和氢离子,亚硫酸氢根离子和氢离子反应生成二氧化硫和水,故C错误;
D、Ca(OH)2溶液中通入过量CO2,注意二氧化碳过量时,会将碳酸盐转化为碳酸氢盐,即2OH-+CO2=2HCO3-,故D错误.
故选B.
点评:本题考查学生离子方程式的正误判断方法,是现在考试的热点,难度不大.
本题难度:一般