1、选择题 下列电离方程式的书写错误的是( )
A.NaHSO4=Na++H++SO42-
B.MgCl2=Mg2++Cl2-
C.Ba(OH)2=Ba2++2OH-
D.Na2SO4=2Na++SO42-
参考答案:B
本题解析:
本题难度:简单
2、选择题 下列电离方程式错误的是( )
A.NaHCO3=Na++H++CO32-
B.NaHSO4=Na++H++SO42-
C.Al2O3
2Al3++3O2-
D.CaCO3=Ca2++CO32-
参考答案:A.NaHCO3为强电解质,电离方程式为NaHCO3=Na++HCO3-,故A错误;
B.NaHSO4为强电解质,电离方程式为NaHSO4=Na++H++SO42-,故B正确;
C.Al2O3为强电解质,电离方程式为Al2O3?熔融?.?2Al3++3O2-,故C正确;
D.CaCO3为强电解质,电离方程式为CaCO3=Ca2++CO32-,故D正确;
故选A.
本题解析:
本题难度:一般
3、选择题 下列叙述中,正确的是( )
A.在AgBr饱和溶液中加入AgNO3溶液,达到平衡时,溶液中Br-浓度降低
B.常温下,某溶液中由水电离出的c(OH-)=1×10-10mol/L,该溶液一定呈酸性
C.FeCl3溶液和Fe2(SO4)3溶液加热蒸干、灼烧都得到Fe2O3
D.用惰性电极分别电解CuCl2溶液和MgCl2溶液分别得到单质Cu和Mg
参考答案:A
本题解析:
本题难度:简单
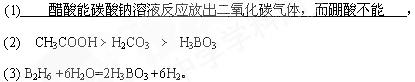
4、填空题 向两支分别盛有0.1mol/L醋酸和饱和硼酸(H3BO3)溶液的试管中滴加等浓度碳酸钠溶液,实验现象为(1) 三种酸由强到弱的顺序是(用化学式表示)(2) ,]硼酸(H3BO3)在食品、医药领域应用广泛。
(3) 请完成B2H6气体与水反应的化学方程式:B2H6 +6H2O=2H3BO3 +________。
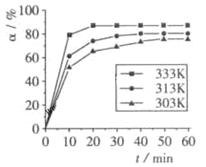
(4) 在其他条件相同时,反应H3BO3 +3CH3OH  B(OCH3)3 +3H2O中,H3BO3的转化率(
B(OCH3)3 +3H2O中,H3BO3的转化率(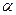 )在不同温度下随反应时间(t)的变化见下图,由此图可得出:
)在不同温度下随反应时间(t)的变化见下图,由此图可得出:
①温度对应该反应的反应速率和平衡移动的影响是____ ___
②该反应的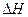 _____0(填“<”、“=”或“>”).
_____0(填“<”、“=”或“>”).
(5) H3BO 3溶液中存在如下反应: H3BO 3(aq)+H2O(l) [B(OH)4]-( aq)+H+(aq)
[B(OH)4]-( aq)+H+(aq)
已知0.70 mol・L-1 H3BO 3溶液中,上述反应于298K达到平衡时,c平衡(H+)="2." 0 × 10-5mol・L-1,c平衡(H3BO 3)≈c起始(H3BO 3),水的电离可忽略不计,此温度下该反应的平衡常数K= ,
(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字)
参考答案:
(4) ①温度升高,H3BO 3的转化率增大,故升高温度是平衡正向移动,正反应是吸热反应
②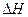 >0
>0
( 5) K= =
=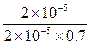 =
=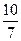 或1.43
或1.43
本题解析:略
本题难度:困难
5、选择题 在常温下10mL pH=10的KOH溶液中,加人一定量的pH=4的一元酸HA溶液至pH刚好等于7,则对反应后溶液的叙述正确的是( )
A.c(HA)+c(A-)=10-4mol/L B.c(H+)=c(OH-)<c(K+)<c(A-)
C.V总≤20mL D.酸和碱一定恰好中和
参考答案:C
本题解析:如果HA为强酸,等体积恰好中和,呈中性,V总=20mL;如果为弱酸,酸的浓度远大于碱的浓度。总体积小于20ml。
本题难度:一般