|
�߿���ѧ֪ʶ���ܽᡶˮ�ĵ���ƽ�⡷����ǿ����ϰ��2019�����°棩(��)
2020-08-13 07:10:48
�� �� �� ��
|
1��ѡ���� �����£��� 0��1000 mol��L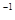 NaOH��Һ�ζ� 20��00mL0��1000 mol��L NaOH��Һ�ζ� 20��00mL0��1000 mol��L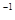 CH3COOH��Һ���õζ�������ͼ������˵����ȷ���� CH3COOH��Һ���õζ�������ͼ������˵����ȷ����
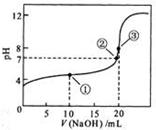
A�������ʾ��Һ�У�c��CH3COO-��+c��OH-��=c��CH3COOH��+c��H+��
B�������ʾ��Һ�У�c��Na+��=c��CH3COOH��+ c��CH3COO-��
C�������ʾ��Һ�У�c��Na+��>c��OH-��>c��CH3COO-��>c��H+��
D���ζ������п��ܳ��֣�
| c��CH3COOH��>c��CH3COO-��>c��H+��>c��Na+��>c��OH-��
�ο��𰸣�D
���������A����ٷ�Ӧ����Һ��CH3COONa��CH3COOH���ʵ���֮��Ϊ1��1�Ļ���CH3COOH����̶ȴ���CH3COO����ˮ��̶ȣ���c��Na+����c��CH3COOH�����ɵ���غ��֪�� c��CH3COO����+c��OH������c��Na+��+c��H+��������c��CH3COO����+c��OH������c��CH3COOH��+c��H+������A����
B�����pH��7����c��H+����c��OH-�����ɵ���غ�֪��c��Na+��+c��H+����c��CH3COO����+c��OH��������c��Na+����c��CH3COO��������B����
C�����˵������Һǡ����ȫ��Ӧ����CH3COONa������CH3COO��ˮ�⣬�ҳ̶Ƚ�С������c��Na+����c��CH3COO������c��OH������c��H+������C����
D����CH3COOH�϶࣬����ļ����ʱ��������CH3COONa���������ܳ���c��CH3COOH����c��CH3COO������c��H+����c��Na+����c��OH��������D��ȷ����ѡD��
���㣺����NaOH��CH3COOH�ķ�Ӧ������Ũ�ȱȽ��Լ��ζ����ߵ�ʶ��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣�����ۺ���ǿ��ע�ش��������ԡ������ѶȽϴ�ѧ����˼ά��������˽ϸߵ�Ҫ���漰�����ˮ�����Һ����Ũ�ȵĴ�С�Ƚϣ�ע�����õ���غ�ĽǶȽ��
�����Ѷȣ�����
2������� ��1�����������ʣ���ͭ �����ᱵ���� �۰�ˮ ���������ƹ��� ����������� ���Ҵ�
��ϡ���� ����ʯ ��������� ������ᡣ
���ڷǵ���ʵ���_____������ǿ����ʵ���_____��������ţ�
��2�������£���pH��3�������pH��11�İ�ˮ�������Ϻ���Һ�� �ԣ���Һ��c��NH4+����c��Cl-���Ĵ�С��ϵ�ǣ�c��NH4+�� c��Cl-�������������
��3�������£�0.010mol��L-1�����0.010mol��L-1��ˮ��pH֮�� 14�������£�pH��2�������pH��12�İ�ˮ���ֱ��ˮϡ��10��������Һ��pH֮�� 14���������
�ο��𰸣���1���ޢ� �ڢܢ� ��2�� �� > ��3�� �� ��
�����������1����ˮ��Һ�л�����״̬���ܵ���Ļ������ǵ���ʣ���ˮ��Һ������״̬�¾�������Ļ�����Ϊ�ǵ���ʣ�����ʵ�������Ϊ�������ˮ��Һ�л�����״̬������������������ƶ����������Ӷ����磻�����ڷǵ���ʵ��Тޢᣬ����ʸ��ݵ���̶ȴ�С��Ϊǿ����ʺ�������ʣ�ǿ�������ȫ�������ǿ�ᡢǿ��ʹ��Σ�������ǿ����ʵ��Тڢܢݣ���2�������£���pH��3�������pH��11�İ�ˮ�������ϣ���Ϻ���Һ����ΪNH4Cl�ʹ�����NH3��H2O�Ļ���NH3��H2O����̶ȴ���Һ�ʼ��ԣ�����Һ��c��NH4+��>c��Cl-������3�������£�0.010mol��L-1�����pH=2��0.010mol��L-1��ˮ������NH3��H2OΪ������ʣ���pH<12��pH֮�ͣ�14����pH��2�������ˮϡ��10��pH��3��pH��12�İ�ˮ��ˮϡ��10����11<pH<12��������Һ��pH֮��>14.
���㣺��Һ������ƽ�⡣
�����Ѷȣ�һ��
3������� (1)���в���ʹ���ƫ�ߣ��������� .
����ϡNaOH��Һ��ϡ���ᷴӦ�ⶨ��Ӧ�ȣ������ʽ�����
���к͵ζ�����ƿ������ˮϴ��δ�ô���Һϴ
����0.1mol��L��1��NaOH��Һ�ζ�δ֪Ũ�ȵ����ᣬ��ʽ�ζ���δ�ñ�Һ��ϴ
��������ˮʪ���pH��ֽ�ⶨ0.1mol��L��1�Ĵ�����Һ��pH
(2)�ڴ�����Һ�е����̪����Һ��졣ԭ���� �������ӷ���ʽ��ʾ�����ڸ���Һ���ٵ���������Ȼ�����Һ�����۲쵽�������� ����ԭ���ǣ������ӷ���ʽ�ͼ�Ҫ����˵������ ��
�ο��𰸣���1���ۢ� ��2�֣� ��2��CO32����H2O  HCO3����OH-��2�֣� HCO3����OH-��2�֣�
������ɫ�������Һ�ɫ��ȥ����2�֣�
�ڴ����м���BaCl2��Һ��Ba2+��CO32����BaCO3¯(��ɫ)��c( CO32��)��С��CO32��ˮ��ƽ�������ƶ���c(OH-)��С����̪��ɫ����2�֣�
���������(1)�۵ζ���δ�ñ�Һ��ϴ����ʹŨ��ϡ�ͣ����õ���ҺҲ�Ͷ࣬�ʻ�ƫ��PH��ֽʪ���ˣ���ϡ�ʹ�����Һ�����Լ�����PH������(2) ������Һ�д�����ǿ�������Σ�ˮ��ɼ��ԣ�����̪�Ժ�ɫ�����ӷ���ʽΪCO32����H2O  HCO3����OH-�������Ȼ�����Һ��Ba2+���CO32����Ӧ��ʹˮ�ⷴӦ�����ƶ������Ծͼ�������ɫ����ȥ�� HCO3����OH-�������Ȼ�����Һ��Ba2+���CO32����Ӧ��ʹˮ�ⷴӦ�����ƶ������Ծͼ�������ɫ����ȥ��
���㣺����һ�����ʵ���Ũ�ȵ���Һ �к͵ζ� PH��ֽ �����ˮ��
������������Ҫ������һЩʵ�����������ˮ���֪ʶ������ʵ���ԭ������ȷ�IJ���������ˮ���ԭ���ǽ���Ĺؼ���
�����Ѷȣ�һ��
4��ѡ���� ����˵������ȷ���ǣ�������
A����ˮ�ܹ����磬�ʰ�ˮ�ǵ����
B�����ᱵ������ˮ�������ᱵ����ǿ�����
C��������̼����ˮ�ܲ��ֵ��룬�ʶ�����̼�����������
D����������ˮ�еĵ��뷽��ʽ�ɱ�ʾΪNa2SO4�T2Na++S6++4O2-
�ο��𰸣�B
���������
�����Ѷȣ���
5��ѡ���� 25��ʱ��ij��Һ�У���ˮ�������c(H+)=1��10-12mol��L-1�������Һ��c(H+)������
[? ]
A��1��10-12 mol��L-1
B��1��10-7 mol��L-1
C��1��10-6 mol��L-1
D��1��10-2 mol��L-1
�ο��𰸣�AD
���������
�����Ѷȣ�һ��
|