1、简答题 如图,在试管a中先加入2mL95%的乙醇,边摇动边缓缓加入5mL浓H2SO4并充分摇匀,冷却后再加入2g无水醋酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管b中加入7mL饱和碳酸钠溶液.连接好装置,用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验.
(1)写出a试管中的主要化学反应的方程式?;
(2)加入浓H2SO4的目的是?.
(3)试管b中观察到的现象是?.
(4)在实验中球形干燥管除起冷凝作用外,另一个重要作用是?.
(5)饱和Na2CO3溶液的作用是?.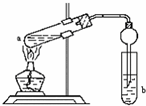
参考答案:(1)装置中发生的反应是利用醋酸钠和浓硫酸反应生成醋酸和乙醇在浓硫酸催化作用下发生酯化反应,生成乙酸乙酯和水,反应的化学方程式为:
2CH3COONa+H2SO4=2CH3COOH+Na2SO4 CH3COOH+CH3CH2OH浓硫酸
本题解析:
本题难度:一般
2、实验题 (28分)
[1]由碳、氢、氧三种元素组成的某有机物分子中共含有13个原子,其原子核外共有40个电子,l mol该有机物在氧气中完全燃烧时需消耗5.5 mol O2。请回答:
(1)试求出该有机物的分子式为 ?。
(2)若该有机物可使溴水褪色,且分子中不含有甲基,也不能发生银镜反应,取0.1 m ol该有机物与足量钠反应,能产生1.12 L H2(标准状况),则该有机物的结构简式可能是?;该有机物在一定条件下发生聚合反应的化学方程式是?。
ol该有机物与足量钠反应,能产生1.12 L H2(标准状况),则该有机物的结构简式可能是?;该有机物在一定条件下发生聚合反应的化学方程式是?。
(3)若该有机物能发生银镜反应,且分子中只含有一个甲基,则其结构简式是?。
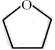
(4)若该有机物的结构呈环状,且既不含甲基又不含羟基,则其键线式是?。
[2]2006年5月,齐齐哈尔第二制药厂生产的假药“亮菌甲素注射液”导致多名患者肾功能衰竭。“亮菌甲素”的结构简式为?,它配以辅料丙二醇?
溶成针剂用于临床。假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强
的毒性。请回答下列问题:
(1)“亮菌甲素”的分子式为?。
(2)丙二醇的分子式是C3H8O2,已知两个羟基连在同一个碳原子上的物质不存在。写出其属于醇类的同分异构体的结构简式??。
(3)下列有关“亮菌甲素”的叙述正确的是??(填序号)。
A.“亮菌甲素”能与H2发生加成反应? B.不能使酸性KMnO4退色
C.“亮菌甲素”分子中含氧官能团只有2种? D.1mol“亮菌甲素”最多与2molNaOH反应
(4)核磁共振氢谱分析,发现二甘醇分子中有3个肿收峰,其峰面积之比为2:2:1。又知二甘醇中C、O元素的质量分数相同,且H的质量分数为9.4%,1mol二甘醇与足量的金属钠反应生成1molH2。写出二甘醇与乙酸(按物质的量之比1:1)反应的化学方程式? ?
?
参考答案:(16)(1)C4H8O
(2)CH2=CHCH2CH2OH
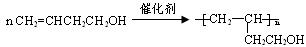 ?
?
(3)CH3CH2CH2CHO
(4)
本题解析:略
本题难度:简单
3、简答题 硫酸是一种重要的化学试剂.某实验小组的同学利用浓硫酸进行制取二氧化硫并探究其性质的实验.请按要求回答下列问题.
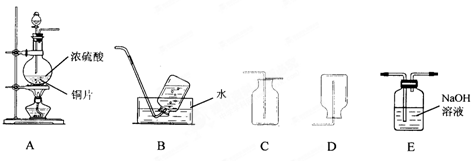
(1)装置A中发生反应的化学方程式为______.上述装置中适于收集二氧化硫的气体是(填字母)______.
(2)将一收集满二氧化硫气体的小试管倒置于滴有紫色石蕊溶液的水中,可观察到的现象是______.
(3)上述实验所产生的二氧化硫尾气可选用E装置来吸收,该反应的化学方程式为______.
参考答案:(1)依据装置图中试剂和物质性质分析是浓硫酸和铜加热反应生成硫酸铜、二氧化硫和水,反应的化学方程式为Cu+2H2SO4(浓)?△?.?CuSO4+2H2O+SO2↑;依据二氧化硫气体易溶于水不能用B,比空气重不能用D,需要用向上排空气法收集,所以选C,
故答案为:Cu+2H2SO4(浓)?△?.?CuSO4+2H2O+SO2↑;C;
(2)将一收集满二氧化硫气体的小试管倒置于滴有紫色石蕊溶液的水中,二氧化硫溶于水和水反应生成亚硫酸,水面上升,亚硫酸是中强酸,遇石蕊变红,
故答案为:试管内液面上升,溶液变成红色;
(3)二氧化硫是污染性气体,排放到空气中污染环境,需要氢氧化钠溶液吸收,反应生成亚硫酸钠和水,反应的化学方程式为2NaOH+SO2=Na2SO3+H2O,
故答案为:2NaOH+SO2=Na2SO3+H2O.
本题解析:
本题难度:一般
4、选择题 下列是有关生活中对醋酸的应用,其中主要利用了醋酸酸性的是(?)
A.醋酸溶液可一定程度上治疗手足癣
B.熏醋可一定程度上防治流行性感冒
C.醋可以除去水壶上的水垢
D.用醋烹饪鱼,除去鱼的腥味
参考答案:C
本题解析:略
本题难度:简单
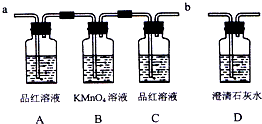
5、填空题 某校研究性学习小组,设计如下装置来验证浓硫酸与木炭在加热条件下的产物中含有SO2和CO2.同学们查阅资料得知二氧化硫可使酸性高锰酸钾溶液褪色,化学方程式为:2KMnO4+5SO2+2H2O=K2SO4+2MnSO4+2H2SO4
(1)写出浓硫酸与木炭在加热的条件下化学反应方程式:______
(2)实验时,反应产生的气体应从______端通入装置.(用“a”或“b”填空)
(3)A瓶的实验现象是______,B瓶溶液的作用是______.
(4)要证明产物中含有CO2的实验现象是:C中品红溶液______,D中澄清石灰水______.
参考答案:(1)根据木炭粉与浓硫酸发生反应书写化学方程式,该反应为C+2H2SO4(浓)△.CO2↑+2SO2↑+2H2O,
故答案为:C+2H2SO4(浓)△.CO2↑+2SO2↑+2H2O;
(2)反应产物含有二氧化碳和二氧化硫气体,都能使澄清石灰水变浑浊,需要先验证二氧化硫的存在,除去二氧化硫,再验证二氧化碳气体的存在,气体通过溶液导气管一个长进短出,所以实验时,反应产生的气体应从a端进入装置;
故答案为:a;
(3)A是验证二氧化硫气体的存在,二氧化硫能使品红溶液褪色,B瓶中酸性高锰酸钾溶液可以除去二氧化硫,化学方程式为:2KMnO4+5SO2+2H2O=K2SO4+2MnSO4+2H2SO4,在检验二氧化碳气体时不受干扰,
故答案为:品红溶液褪色;除尽SO2;
(4)当C装置品红不褪色,证明二氧化硫气体除净,D装置中澄清石灰水变浑浊证明含有二氧化碳;
故答案为:不褪色;变浑浊.
本题解析:
本题难度:简单