1、选择题 下列物质中,不能做漂白剂的是
[? ]
A.SO2
B.Ca(ClO)2
C.NaClO
D.H2SO4
参考答案:D
本题解析:
本题难度:简单
2、选择题 由下列实验事实得出结论不正确的是( )
A.蔗糖加入浓硫酸后变黑,说明浓硫酸具有脱水性
B.浓硫酸可用作气体干燥剂,说明浓硫酸具有吸水性
C.铜与浓硫酸共热有刺激性气味气体放出,说明浓硫酸具有强氧化性
D.SO2能使紫红色的酸性高锰酸钾溶液褪色,说明SO2具有漂白性
参考答案:A.浓硫酸具有脱水性,可使蔗糖碳化而变黑,故A正确;
B.浓硫酸具有吸水性,可用作干燥剂,但不能干燥碱性或强还原性的气体,故B正确;
C.浓硫酸具有强氧化性,在加热条件下可与铜发生氧化还原反应生成硫酸铜和二氧化硫气体,故C正确;
D.二氧化硫具有还原性,与酸性高锰酸钾发生氧化还原反应,故D错误.
故选D.
本题解析:
本题难度:简单
3、选择题 1?丁醇CH3CH2CH2CH20H和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125 ℃,反应装置如图,下列对该实验的描述错误的是
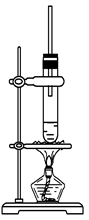
A.不能用水浴加热
B.长玻璃管起冷凝回流作用
C.1?丁醇和乙酸能反应完或者有一种能消耗完
D.加入过量乙酸可以提高1?丁醇的转化率
参考答案:C
本题解析:因为反应需要反应温度为115~125℃,而水浴加热适合温度低于100℃的反应,故A正确;有易挥发的液体反应物时,为了避免反应物损耗和充分利用原料,要在发生装置设计冷凝回流装置,使该物质通过冷凝后由气态恢复为液态,从而回流并收集.实验室可通过在发生装置安装长玻璃管或冷凝回流管等实现,故B正确;酯化反应是可逆反应,故1?丁醇和乙酸不可能完全反应,所以C错误,为本题的正确答案;酯化反应为可逆反应,增加乙酸的量,可使平衡向生成酯的方向移动,从而提高1-丁醇的转化率,故D正确,所以本题的答案选择C。
点评:本题考查了酯的制取,掌握乙酸乙酯的制取是类推其他酯的制取的基础,注意装置中各部分的作用及酯的性质来解答.
本题难度:一般
4、填空题 硫酸的性质有:A.高沸点;B.强酸性;C.吸水性;D.脱水性;E.强氧化性.在下列硫酸的用途或化学反应中,硫酸可能表现上述的一个或者多个性质,试用字母填空:
(1)实验室制取氢气______;
(2)实验室干燥氢气______;
(3)浓硫酸与金属铜的反应______;
(4)实际生产中,浓硫酸可用钢瓶贮运______;
(5)碳粉与热的浓硫酸反应放出有刺激性气味的气体______.
(6)浓硫酸使蓝色胆矾晶体(CuSO4?5H2O)变白色______.
参考答案:(1)稀硫酸和金属反应制取氢气是硫酸的强酸性,所以实验室用锌与盐酸制氢气表现了硫酸的强酸性,故选:B;
(2)做干燥剂是浓硫酸的吸水性,所以实验室用浓硫酸干燥氢气,体现了硫酸的吸水性,故选:C;
(3)稀硫酸和铜不反应,浓硫酸和铜在加热条件下反应,体现浓硫酸的酸性和强氧化性,故选:BE;
(4)实际生产中,浓硫酸可用钢瓶贮运,金属产生钝化现象,体现浓硫酸的强氧化性,故选:E;
(5)碳粉与热的浓硫酸反应放出有刺激性气味的气气体,体现浓硫酸的强氧化性,故选:E;
(6)浓硫酸使蓝色胆矾晶体(CuSO4?5H2O)变白色体现了浓硫酸的吸水性,故选:C.
本题解析:
本题难度:简单
5、简答题 [化学-化学与技术]硫酸工业生产应考虑综合经济效益问题.
(1)若从下列四个城市中选择一处新建一座硫酸厂,你认为厂址宜选在______的郊区(填标号);
A.有丰富黄铁矿资源的城市
B.风光秀丽的旅游城市
C.消耗硫酸甚多的工业城市
D.人口稠密的文化、商业中心城市
(2)CuFeS2是黄铁矿的另一成分,煅烧时CuFeS2转化为CuO、Fe2O3和SO2,该反应的化学方程式为______.
(3)在硫酸工业制法中,下列生产操作与说明生产操作的主要原因二者都是正确的是______.
A.黄铁矿燃烧前需要粉碎,因为大块的黄铁矿不能在空气中燃烧
B.从沸腾炉出来的炉气需净化,因为炉气中二氧化硫会与杂质反应
C.二氧化硫氧化为三氧化硫时需使用催化剂,这样可以提高二氧化硫的转化率
D.三氧化硫用98.3%的浓硫酸吸收,目的是防止形成酸雾,以提高三氧化硫的吸收效率
(4)由硫酸厂沸腾炉排出的矿渣中含有Fe2O3、CuO、CuSO4(由CuO与SO3在沸腾炉中化合而成),其中硫酸铜的质量分数随沸腾炉温度不同而变化(见下表)
| 沸腾炉温度/℃ | 600 | 620 | 640 | 660
炉渣中CuSO4的质量分数/%
9.3
9.2
9.0
8.4
|
已知CuSO4在低于660℃时不会分解,请简要分析上表中CuSO4的质量分数随温度升高而降低的原因______.
参考答案:(1)A.硫酸厂厂址的选择综合经济效益考虑,硫酸产品的运输成本要高于原料黄铁矿的运输成本.故A不正确;
B.风光秀丽的旅游城市,不靠近原料基地,也不靠近消耗硫酸的工业城市,导致原料运输与产品运输成本高,同时还会对旅游城市造成污染.故B不正确;
C.由于硫酸产品的运输成本要高于原料黄铁矿的运输成本,所以厂址应选择在消耗硫酸甚多的工业城市.故C正确;
D.人口稠密的文化、商业中心城市,远离原料基地和消耗硫酸的工业城市,同时为了防止污染环境,不宜考虑作为硫酸厂厂址.故D不正确;
故答案为:C;
(2)根据题意可知,高温煅烧时CuFeS2时,反应物为CuFeS2和O2,生成物为CuO、Fe2O3和SO2,再根据化合价升降法配平氧化还原反应方程式,
故答案为:4CuFeS2+13O2煅烧.4CuO+2Fe2O3+8SO2;
(3)A.在硫酸工业制法中,黄铁矿燃烧前需要粉碎,是为了增大与空气的接触面,加快反应速率,不是因为大块的黄铁矿不能在空气中燃烧.故A不正确;
B.从沸腾炉出来的炉气中含有SO2、O2、N2、水蒸气、灰尘、砷硒化合物等,由于砷硒化合物能导致催化剂失去催化活性,因此需净化,不是因为炉气中二氧化硫会与杂质反应,故B不正确;
C.二氧化硫氧化为三氧化硫时需使用催化剂,目的是加快反应速率,提高产量.并不能提高二氧化硫的转化率,故C不正确;
D.在吸收塔中三氧化硫用98.3%的浓硫酸吸收,目的是防止形成酸雾,以提高三氧化硫的吸收效率.故D正确;
故答案为:D;
(4)硫酸厂沸腾炉排出的矿渣中含有Fe2O3、CuO、CuSO4(由CuO与SO3在沸腾炉中化合而成),根据题意由表中数据可知,硫酸铜的质量分数随沸腾炉温度升高而降低,是因为反应CuO+SO3△.CuSO4中SO3的质量减少导致的,根据2SO2(g)+O2(g)催化剂
本题解析:
本题难度:一般