1、选择题 下图表示某物质发生的是
参考答案:B
本题解析:根据模型可知,该反应是醋酸根离子的水解反应,答案选B。
点评:盐电离出来的离子结合水电离出来的 H+或 OH-生成弱电解质的过程称为盐类水解,据此可以判断。
本题难度:一般
2、选择题 下列过程或现象与盐类水解无关的是
A.铁在潮湿的环境下生锈
B.纯碱溶液去油污
C.加热氯化铁溶液颜色变深
D.草木灰不宜与用作氮肥的铵盐使用
参考答案:A
本题解析:A:铁生锈(电化学腐蚀)的必须条件之一即是有水的存在,而与盐类的水解无关
B:纯碱水解可生成碱液,可与油污发生皂化反应而生成可溶于水的物质而达到去污的目的
C:盐类的水解是吸热反应,加热促进氯化铁水解
D:两者分属于碳酸盐、铵盐,易互相促进水解,而导致肥力的浪费
故选A
本题难度:简单
3、填空题 某同学想把AlCl3溶液和Na2S溶液混合制取Al2S3,但最后得到一种白色絮状沉淀,并且混合液中有臭鸡蛋气味的气体放出。试解释造成此结果的原因,写出反应的离子方程式,并指出制取硫化铝的正确方法。
参考答案:Ⅰ?①增强②Fe2O3③减小减弱④溶液变红⑤生成无色气体,Mg片漂浮生成红褐色沉淀。
Ⅱ?在溶液中Al3+、S2-水解互相促进,发生剧烈水解。2Al3++3S2-+6H2O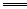 2Al(OH)3↓+3H2S↑H2S有臭鸡蛋气味。用S粉与Al粉(混合均匀)在干态时共热可制取Al2S32Al+3S
2Al(OH)3↓+3H2S↑H2S有臭鸡蛋气味。用S粉与Al粉(混合均匀)在干态时共热可制取Al2S32Al+3S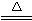 Al2S3
Al2S3
本题解析:Ⅰ?FeCl3溶液中存在下列平衡:
Fe3++3H2O Fe(OH)3+3H+
Fe(OH)3+3H+
加入NaOH中和H+,水解平衡右移。通入HCl(g)增大c(H+)使平衡左移,水解显酸性,滴入石蕊变红,加入MgCl2产生H2气泡,且平衡右移,生成Fe(OH)3沉淀。
蒸干FeCl3溶液,水解平衡右移,HCl挥发,生成Fe(OH)3沉淀,最后灼烧完全分解,所得固体为Fe2O3。
本题难度:简单
4、选择题 0.1 mol?L-1 KHCO3溶液中下列表达式不正确的是
A.c(K +)+c(H+)= c(OH-)+ c(HCO3-)+2 c(CO32-)
B.c(K+)> c (HCO3-)> c(OH-)> c(CO32-)> c(H+)
C.c(HCO3-)+ c(CO32-)+ c(H2 CO3)=" 0.1" mol?L-1
D.c(K+)> c(HCO3-)> c(OH-)> c(H+)> c(CO32-)
参考答案:B
本题解析:A正确,符合电荷守恒;碳酸氢钾的水解程度大于电离程度,溶液显碱性,B不正确,因为水还存在电离平衡,应该是c(K+)> c (HCO3-)> c(OH-)> c(H+)> c(CO32-),所以D不正确;C正确,符合物料守恒,答案选B。
点评:该题的关键是记住碳酸氢钾的水解程度大于电离程度,然后在依据电荷守恒、物料守恒和质子守恒进行判断。
本题难度:一般
5、填空题
(10分)(1)AgNO3的水溶液呈?(填“酸”、“中”、“碱”)性,常温时的pH ?7(填“>”、“=”、“<”),原因是(用离子方程式表示):?;?实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以?(填“促进”、“抑制”)其水解。
(2)氯化铝水溶液呈?性,原因是(用离子方程式表示):?________________ 。
把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是??。
(3)在配制硫化钠溶液时,为了防止发生水解,可以加入少量的??。
参考答案:(10分)(方程式2分,其余1分)
(1)酸,<,Ag++ H2O 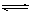 ?AgOH + H+,抑制。
?AgOH + H+,抑制。
(2)酸,Al3++3H2O 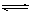 ?Al(OH)3+3H+, Al2O3?;
?Al(OH)3+3H+, Al2O3?;
(3)NaOH
本题解析:(1)AgNO3为强酸弱碱盐,水溶液呈酸性,常温时的pH <7,原因是:Ag++ H2O 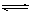 ?AgOH + H+,实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以抑制其水解。
?AgOH + H+,实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以抑制其水解。
(2)氯化铝为强酸弱碱盐,水溶液呈酸性,其原因是:Al3++3H2O 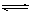 ?Al(OH)3+3H+,当把把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是Al2O3;
?Al(OH)3+3H+,当把把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是Al2O3;
(3)硫化钠溶液为强碱弱酸盐,水溶液呈碱性,为了防止发生水解,可以加入少量的NaOH
本题难度:一般