1、推断题 有三种坚硬、不溶于水的透明固体,A固体在氧气中完全燃烧只生成一种无色气体,此气体能使澄清石灰水变浑浊,该气体的密度是相同条件下氧气密度的1. 375倍;B固体能溶于热的苛性钠溶液,向该生成物中加入过量盐酸时,又析出白色胶状沉淀,此沉淀干燥失水后为不溶于水的白色粉末,且酸性比碳酸弱;C物质是将B物质与石灰石、纯碱按比例加热后得到的产物,C无固定熔沸点,加热时逐渐软化。据此判断:
(1)A、B、C的名称分别是:A___, B____,C____。
(2)写出此题中涉及的化学反应方程式______________。
参考答案:(1)金刚石 ;石英 ;普通玻璃
(2)C+O2 CO2,
CO2,
CO2+Ca(OH)2=CaCO3↓
SiO2+2NaOH=Na2SiO3+H2O
2HCl+H2O+Na2SiO3=2NaCl+H4SiO4↓
H4SiO4=H2SiO3+H2O
SiO2+CaCO3 CaSiO3+CO2↑
CaSiO3+CO2↑
SiO2+Na2CO3 Na2SiO3+CO2↑
Na2SiO3+CO2↑
本题解析:
本题难度:一般
2、填空题 (12分)Ⅰ.某些化学反应可表示为:A+B→C+D+H2O。请回答下列问题:
(1)若A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,该反应离子方程式为____________?________。
(2)若A为黑色固体,C、D均为气体,则该反应的化学方程式为_____?___。
(3)若C为NaCl,D是能使澄清石灰水变浑浊的无色有刺激性气味的气体,若A为盐,B为酸,则A是?或__?____(填化学式)。
(4)若A是铁的一种氧化物,B是硫酸,则A与B反应的化学方程式为_?___。
Ⅱ.某些化学反应可表示为:A+B +H2O→C+D。请回答下列问题:
若反应物与生成物中各有一种物质含有Si元素,请写出2个符合要求的化学反应方程式
?,?
参考答案:Ⅰ(1)Cl2+2OH-=Cl-+ClO-+H2O
(2)若A为黑色固体,C、D均为气体,则A应该是碳,B是浓硫酸,所以反应的化学方程式是C+2H2SO4(浓)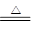 CO2↑+SO2↑+2H2O。
CO2↑+SO2↑+2H2O。
(3)D是能使澄清石灰水变浑浊的无色有刺激性气味的气体,所以D是SO2,因此B是盐酸,则A是Na2SO3或NaHSO3。
(4)若A是铁的一种氧化物,B是硫酸,则根据生成物有两种硫酸盐可知,A应该是四氧化三铁,所以反应的方程式是Fe3O4+4H2SO4=FeSO4+Fe2(SO4)3+4H2O。
ⅡNa2SiO3+CO2+H2O=H2SiO3↓+Na2CO3((或NaHCO3)、Si+2NaOH+H2O= Na2SiO3+2H2↑
本题解析:Ⅰ(1)若A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,所以A应该是氯气,B是氢氧化钠,则反应的离子方程式是Cl2+2OH-=Cl-+ClO-+H2O。
(2)C+H2SO4=CO2+SO2+H2O
(3)Na2SO3? NaHSO3
(4)Fe3O4+4H2SO4=FeSO4+Fe2(SO4)3+4H2O
Ⅱ反应物与生成物中各有一种物质含有Si元素,所以该反应可以是可溶性硅酸盐和酸反应制取硅酸的,或者是单质硅和强碱溶液的反应,因此方程式分别是Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3((或NaHCO3)、Si+2NaOH+H2O= Na2SiO3+2H2↑。?
点评:在根据方程式进行物质的判断时,需要熟练掌握各种物质的性质,特别是化学性质,以及物质之间的转化,然后灵活运用即可。
本题难度:一般
3、填空题 下图所示各物质是由1~20号元素中部分元素组成的单质或其化合物,图中部分反应条件和产物未列出。已知C、D、E、H是常见的气体且D为单质。反应②和④是化工生产中的重要反应,反应⑤是实验室制备气体C的重要方法,反应⑥是J的失效反应原理。 ?
?
请回答下列问题:
⑴物质L的电子式为____________,E的结构式为_______________。
⑵D所含元素位于周期表__________________,生产D的工业被称为_______________。
⑶反应⑤的化学方程式为___________________________________________。
反应⑥的离子方程式为___________________________________________。
⑷物质A由三种元素组成,1molA与水反应可生成1molB和2molC,A的化学式为________。
参考答案:⑴? ?O=C=O(2分)⑵第三周期VIIA族,氯碱工业(2分)
?O=C=O(2分)⑵第三周期VIIA族,氯碱工业(2分)
⑶Ca(OH)2+2NH4Cl ?CaCl2+2NH3↑+2H2O(2分)
?CaCl2+2NH3↑+2H2O(2分)
Ca2++2ClO―+CO2+H2O=CaCO3↓+2HClO(2分)? ⑷CaCN2(2分)
本题解析:本题突破口为:反应⑥是J的失效反应原理,中学阶段只有漂白粉符合题意,∴J为Ca(ClO)2。又知D为常见气体单质,D+I→J+K+H2O,且反应②④是工业生产中的重要反应,可推知,D为Cl2,I为Ca(OH)2,④是工业制漂白粉的重要反应。∵F+H2O→I,∴F为CaO, B为CaCO3,②为工业煅烧石灰石。再由反应⑤是实验室制备气体C的重要方法,I+G →C+K+H2O∴C为氨气,G为NH4Cl,C+H→NH4Cl,所以H为HCl。本题难点是确定物质A组成,由1molA与水反应生成1molB和2molC知:A+H2O→CaCO3+2NH3,据原子守恒知H2O系数为3,∴A为CaCN2。
本题难度:一般
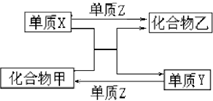
4、选择题 X、Y、Z是三种常见的单质,甲、乙是两种常见的化合物.下表各组物质之间通过一步反应不能实现如图所示转化的是(依次为X、Y、Z、甲、乙)( )
A.H2、Si、Cl2、SiCl4、HCl
B.Mg、C、O2、CO2、MgO
C.Zn、Fe、Cl2、FeCl2、ZnCl2
D.O2、N2、H2、NH3、H2O