|
|
|
���л�ѧ֪ʶ���ܽᡶ�Ȼ�ѧ����ʽ������Ԥ�⣨2020�����°棩(��)
2020-08-23 06:22:48
�� �� �� ��
|
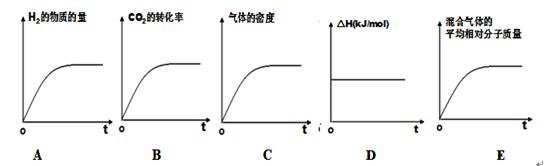
1������� ��15�֣��о�̼���仯��������Ҫ���塣
��1����ѧ����CO2��H2�����״���ȼ�ϡ�
��֪���״���ȼ���Ȧ�H= -726.5kJ/mol��������ȼ���Ȧ�H= -285.8kJ/mol��
���³�ѹ�£�CO2(g)��H2(g)��Ӧ����CH3OH(l)���Ȼ�ѧ����ʽ ��
��2��460��ʱ����4L�ܱ������г���1mol CO2��3.25mol H2����һ�������·�Ӧ�����CO2��CH3OH(g)�����ʵ�����ʱ��ı仯��ϵ��ͼ��ʾ��
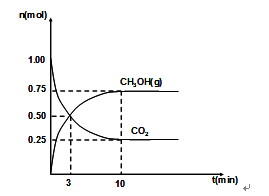
�ٴӷ�Ӧ��ʼ��3minʱ��H2O(g)��ƽ����Ӧ���� ��
�����д�ʩ�м��ܼӿ췴Ӧ��������ʹH2��ת����������� ��
A��ʹ�ø���Ч�Ĵ���
B����ԭ�������ٳ���1mol CO2
C����ԭ�������ٳ���1mol He
D�������������
| E�����״���ʱ�������
�����÷�Ӧ���ʱ�Ϊ��H��������ʾ��ͼ��ȷ����˵����Ӧ�ﵽƽ��״̬����________��
�ܸ������£��˷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ ��
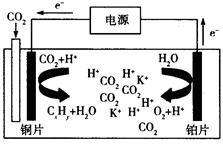
��3����ѧ���о����֣��������õ������CO2��ԭΪ̼�⻯���ԭ������ͼ��ʾ���������Һ��һ�ּ��Σ�����CxHyΪC2H4�����ԭ�����ܷ�ӦʽΪΪ�� ��
��4����֪
��ѧʽ
| ����ƽ�ⳣ��
| HCN
| K=4.9��10-10
| H2CO3
| K1=4.3��10-7��K2=5.6��10-11
|
��25��ʱ�����HCN��NaCN�Ļ����Һ��pH=11����c(HCN)/c(CN-)=_________��
����NaCN��Һ��ͨ������CO2��������Ӧ�����ӷ���ʽΪ��________________��
2������� ��֪�����Ȼ�ѧ����ʽ��
��1��C��s��ʯī��+O2��g���TCO2��g����H=-393.5kJ?mol-1
��2��2H2��g��+O2��g���T2H2O��l����H=-571.6kJ?mol-1
��3��2C2H2��g��+5O2��g���T4CO2��g��+2H2O��l����H=-2599kJ?mol-1
��д��C��s��ʯī����H2��g������1mol C2H2��g�����Ȼ�ѧ����ʽ______��
3������� ����(H2NCONH2)��һ�ַdz���Ҫ�ĸߵ����ʣ��ڹ�ũҵ���������ŷdz���Ҫ�ĵ�λ��
��1����ҵ�Ϻϳ����صķ�Ӧ���£�
2NH3(l)+CO2(g)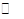 H2O(l)+H2NCONH2(l) ��H=-103��7 kJ��mol-1 H2O(l)+H2NCONH2(l) ��H=-103��7 kJ��mol-1
���д�ʩ��������������ص��������ʵ���
A�����ø���
B�����ø�ѹ
C��Ѱ�Ҹ���Ч�Ĵ���
D����С��ϵ��CO2Ũ��
|
��2���ϳ����صķ�Ӧ�ڽ���ʱ��Ϊ����������
��һ����2NH3(l)+CO2(g)
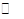
H2NCOONH4(���������)(l) ��H1
�ڶ�����H2NCOONH4(l)
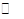
H2O(l)+H2NCONH2(l) ��H2��
ijʵ��С��ģ�ҵ�Ϻϳ����ص���������һ���Ϊ0��5 L�ܱ�������Ͷ��4 mol����l mol������̼��ʵ���÷�Ӧ�и������ʱ��ı仯����ͼI��ʾ��
����֪�ܷ�Ӧ�Ŀ���������һ����������ϳ������ܷ�Ӧ�Ŀ����ɵ�
����Ӧ�������ܷ�Ӧ���е�
minʱ����ƽ�⡣
�ڵڶ�����Ӧ��ƽ�ⳣ��K���¶ȵı仯����ͼII��ʾ�����H2
0(�>�� ��<�� �� ��=��)
��3�����¶�70-95��ʱ����ҵβ���е�NO��NO2������������Һ���գ�����ת��ΪN2
��������NO��NO2���ߵ����ʵ�����Ӧ����ѧ����ʽΪ
����֪��N2(g)+O2(g)=2NO(g)����H=180��6 kJ��mol-1
N2(g)+3H2(g)=2NH3(g) ��H=-92��4 kJ��mol-1
2H2(g)+O2(g)=2H2O(g) ��H=-483��6 kJ��mol-1
��4NO(g)+4NH3(g)+O2(g)=4N2(g)+6H2O(g) ��H=
kJ��mol-1
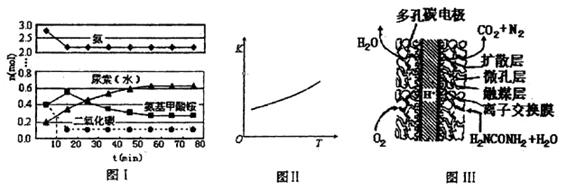
��4������ȼ�ϵ�ؽṹ����ͼIII��ʾ���乤��ʱ�����缫��Ӧʽ
�ɱ�ʾΪ
��
4��ѡ���� 1g̼������ˮ������Ӧ����CO��H2��������10.94kJ�������˷�Ӧ���Ȼ�ѧ����ʽΪ�� ��
A��C + H2O ="=" CO + H2��H= +131.28kJ��mol-1
B��C(s)+ H2O(g) ="=" CO(g) + H2(g)��H= +10.94 kJ��mol-1
C��C(s)+ H2O(l) ="=" CO(g) + H2(g)��H= +131.28kJ��mol-1
D��C(s)+ H2O(g) ="=" CO(g) + H2(g)��H= +131.28kJ��mol-1
5������� 4���������������ȫȼ��ʱ�ų�37ǧ���������÷�Ӧ���Ȼ�ѧ����ʽ�ǣ�_____________ ��


 H2NCOONH4(���������)(l) ��H1
H2NCOONH4(���������)(l) ��H1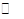 H2O(l)+H2NCONH2(l) ��H2��
H2O(l)+H2NCONH2(l) ��H2��